- Tétrahydrothiophène
-
Tétrahydrothiophène 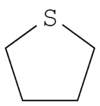
Tétrahydrothiophène Général Synonymes THT
Sulfure de tétraméthylène
Thiolane
ThiophaneNo CAS No EINECS SMILES InChI Apparence liquide incolore, d'odeur caractéristique[1]. Propriétés chimiques Formule brute C4H8S [Isomères] Masse molaire[3] 88,171 ± 0,009 g·mol-1
C 54,49 %, H 9,15 %, S 36,37 %,Moment dipolaire 1,90 D [2] Diamètre moléculaire 0,539 nm [2] Propriétés physiques T° fusion -96,2 °C[1] T° ébullition 119 à 121 °C[1] Solubilité dans l'eau : nulle Masse volumique 1,0 g·cm-3[1] T° d'auto-inflammation 200 °C[1] Point d’éclair 12 °C[1] Limites d’explosivité dans l’air 1,1–12,3 %vol[1] Point critique 358,85 °C [4] Thermochimie Cp Propriétés optiques Indice de réfraction  1,502 [2]
1,502 [2]Précautions Directive 67/548/EEC 
Xn
FPhrases R : 11, 20/21/22, 36/38, 52/53, Phrases S : (2), 16, 23, 36/37, 61, Transport - 2412 SGH[6] 

DangerÉcotoxicologie LogP 1,8[1] Unités du SI & CNTP, sauf indication contraire. Le tétrahydrothiophène ou thiolane ou encore régulièrement désigné sous l'acronyme THT, est un composé organique hétérocyclique. C'est un thioéther cyclique à cinq atomes, un de soufre et quatre de carbone. C'est le composé le plus simple de la famille des thiolanes.
C'est un gaz incolore et inflammable, avec une odeur très caractéristique, si bien qu'il est ajouté dans le gaz consommable pour déceler d'éventuelles fuites.
Références
- TETRAHYDROTHIOPHENE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, 1999, 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Properties of Various Gases sur flexwareinc.com. Consulté le 12 avril 2010
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co. (ISBN 0-88415-857-8)
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
Catégories :- Produit chimique nocif
- Produit chimique facilement inflammable
- Produit chimique dangereux pour l'environnement
- Thiolane
Wikimedia Foundation. 2010.



