- Tétrafluorométhane
-
Tétrafluorure de carbone
 Pour les articles homonymes, voir R14.
Pour les articles homonymes, voir R14.Tétrafluorure de carbone 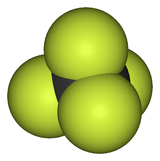
Général Nom IUPAC Tétrafluorure de carbone Synonymes tétrafluorométhane
Perfluorométhane
Fréon 14,
Halon 14,
Arcton 0,
CFC 14,
PFC 14,
R 14No CAS No EINECS PubChem SMILES InChI Apparence gaz comprimé incolore sans odeur.[1] Propriétés chimiques Formule brute CF4 [Isomères] Masse molaire 88,0043 g∙mol-1
C 13,65 %, F 86,35 %,Propriétés physiques T° fusion -183,6 °C[1] T° ébullition -127,8 °C[1] Solubilité 0.005 %V à 20 °C
0.0038 %V à 25 °CMasse volumique 3.72 g/l, gaz (15 °C) T° d’auto-inflammation >1 100 °C[1] Pression de vapeur saturante 3.65 MPa (15 °C)
106.5 kPa (-127 °C)Précautions Directive 67/548/EEC Phrases S : 38, Transport - 1982 SIMDUT[2] 
Unités du SI & CNTP, sauf indication contraire. Le Tétrafluorure de carbone (CF4) ou Perfluorométhane ouTétrafluorométhane ou Fréon 14 ou R 14 ou Halon 14 ou CF4 est un gaz fluoré.
C'est le perfluorocarbure (PFC) le plus abondant dans l'atmosphère terrestre où il contribue à l'effet de serre : son potentiel de réchauffement de la planète (PRP) est 6 500 fois plus élevé que celui du dioxyde de carbone. Sa concentration dans l'atmosphère s'élève désormais à 0,070 ppb en volume.[3].
Sommaire
Composés apparentés ou proches
Voir aussi
Liens externes
Notes et références
- ↑ a , b , c et d TETRAFLUOROMETHANE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Tétrafluorure de carbone » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Page de l'EPA(Agence américaine de protection de l’environnement), citant le GIEC, concernant le potentiel de différents gaz en termes de réchauffement climatique
- Portail de la chimie
Catégories : Composé du fluor | Gaz à effet de serre | Réfrigérant | Perfluorocarbure | Halogénométhane
Wikimedia Foundation. 2010.
