- Rosiglitazone
-
Rosiglitazone 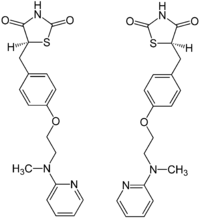
Énantiomères de la rosiglitazone Général No CAS Code ATC BG02 SMILES InChI Propriétés chimiques Formule brute C18H19N3O3S [Isomères] Masse molaire[1] 357,427 ± 0,022 g·mol-1
C 60,49 %, H 5,36 %, N 11,76 %, O 13,43 %, S 8,97 %,Unités du SI & CNTP, sauf indication contraire. La rosiglitazone, commercialisée sous le nom d'Avandia (r), fait partie d'une classe d'antidiabétique oral apparue sur le marché en 2002 : les thiazolidinediones.
Son AMM a été suspendue[2] en France et en Europe en septembre 2010 en raison d'importants risques cardiovasculaires. Aux États-Unis, son utilisation a été fortement restreinte par la FDA[3] pour les mêmes raisons.Sommaire
Mode d'action
Le mode d'action diffère des autres antidiabétiques. La rosiglitazone agit sur le récepteur PPAR gamma, ce qui induit une augmentation de la sensibilité des cellules à l'insuline, et donc une meilleure utilisation de cette dernière. La rosiglitazone agit sur les adipocytes (cellules graisseuses), les hépatocytes (cellules du foie), et les cellules musculaires.
Efficacité
Ainsi l'HbA1c, principal indicateur de la gravité du diabète, peut être réduit de façon sensible. Au cours des essais cliniques, la rosiglitazone a augmenté le HDL-cholestérol et le LDL-cholestérol[4]. La Haute Autorité de santé (HAS) française n’a retrouvé aucune donnée sur la capacité de cette molécule à prévenir ou stabiliser la microangiopathie diabétique[4].
La rosiglitazone permettrait de diminuer sensiblement le risque du sujet pré-diabétique d'évoluer vers un diabète vrai[5].
Effets indésirables et retrait du marché
La Rosiglitazone n'entraîne pas d'hypoglycémie sauf en association avec les sulfamides hypoglycémiants. Elle ne peut pas être prescrite aux patients insuffisants cardiaques quel qu'en soit le degré (classe I à IV de la NYHA, en raison de la rétention hydro-sodée et d'une augmentation de la perméabilité capillaire pulmonaire[4]) ou aux insuffisants hépatiques ni en cas de grossesse. Elle est souvent associée à d'autres antidiabétiques oraux.
En mai 2007, le New England Journal of Medicine avait publié une méta-analyse de 42 études qui démontrait que le risque de crise cardiaque était 43 pour cent plus élevé chez les patients prenant de l'Avandia que chez les autres[6]. À ce moment, Glaxo a émis un communiqué, approuvé par le ministère fédéral de la Santé, qui affirmait que les patients qui prenaient de l'Avandia ne devraient pas cesser de le faire sans tout d'abord consulter leur médecin.
Elle augmente cependant le risque de survenue d'infarctus du myocarde[7], majorant le risque de décès cardio-vasculaire [8] contrairement à une précédente évaluation[9]. Des chercheurs de l’Institut de Sciences Cliniques Evaluatives de Toronto ont mené une étude à partir de la base des données de l’assurance-maladie d’Ontario, incluant 159,026 diabétiques âgés d’au moins 66 ans, suivis en moyenne pendant 3,8 ans, jusqu’en mars 2006, évaluant les risques d’infarctus du myocarde, d’insuffisance cardiaque congestive et de décès. Les patients traités par thiazolidinediones ont des risques accrus de 60% d’insuffisance cardiaque congestive, de 40% d’infarctus du myocarde, de 29% de décès, en comparaison avec des patients traités par d’autres antidiabétiques[10]. « les risques des thiazolidinediones l’emportent sur les bénéfices, même chez les patients qui n’avaient pas de maladies cardio-vasculaires évidentes au départ », disent les chercheurs. Le risque de décès est augmenté par les thiazolidinediones non seulement en monothérapie, mais aussi en thérapie combinée (avec d’autres antidiabétiques). Cela accentue la relation de cause à effet avec cette classe de médicaments et contraste avec la diminution de la morbi-mortalité induite par les autres antidiabétiques. En outre, même une utilisation passée de TZD accroît le risque de décès. Les diabétiques traités par TZD avaient une mortalité augmentée toutes causes confondues, c’est-à-dire non seulement par infarctus du myocarde ou insuffisance cardiaque congestive. Enfin, la mortalité des diabétiques de cette cohorte était indépendante de l’état cardiovasculaire avant le début du traitement ou de la durée du diabète. Ce qui veut dire que des diabétiques qui n’avaient pas de symptômes cardiovasculaires et/ou qui avaient un diabète récent, donc a priori sans complications, ont pu tout autant subir ce type d’effets indésirables des TZD ou décéder. Les résultats de l’étude s’inscrivent donc en faux contre ce qui était affirmé jusqu’ici, à savoir que les TZD seraient à manier avec prudence uniquement chez les personnes à haut risque d’insuffisance cardiaque congestive. Aucun sous-groupe n’a été protégé des effets indésirables d’Avandia et d’Actos. Résumé original de l’étude et références : Thiazolidinediones and Cardiovascular Outcomes in Older Patients With Diabetes, Lipscombe et all, JAMA, 298(22), 12 December 2007, p 2634–2643 [11].
Ces faits ont remis en cause pour les autorités l'intérêt de cette molécule[12], jusqu'à plus amples études. Cette majoration du risque est peut-être liées à la classe des thiazolidinedione[13] , mais d'autres molécules de cette dernière semblent ne pas compromettre le système cardio-vasculaire [14],[15]. → Plusieurs sociétés savantes émettent, en 2008, des avis défavorables quant à la poursuite de l'utilisation de cette molécule[16].
Cela aboutit à la suspension de l'AMM en Europe en septembre 2010[2].
En juillet 2010, GSK a même été soupçonné d'avoir tenté de dissimuler un certain nombre d'effets indésirables[17]
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- Communiqué de l'AFSSAPS du 23 septembre 2010 [1]
- Dépêche de l'Associated Press du 23 septembre 2010 [2]
- Traitement médicamenteux du diabète de type 2 (actualisation 2006) Recommandation de bonne pratique de la Haute Autorité de santé française
- (en)Effect of rosiglitazone on the frequency of diabetes in patients with impaired glucose tolerance or impaired fasting glucose: a randomised controlled trial, The DREAM (Diabetes REduction Assessment with ramipril and rosiglitazone Medication) Trial Investigators, The Lancet 2006; 368:1096-1105
- [3]
- Nissen SE, Wolski K, Effect of Rosiglitazone on the risk of myocardial infarction and death from cardiovascular causes, New Eng J Med, 2007:356:2457-2471
- [4]
- Long-term risk of cardiovascular events with rosiglitazone: A meta-analysis, Singh S, Loke YK, Furberg CD, JAMA, 2007;298:1189-1195
- [5]
- [6]
- Psaty BM, Furberg CD, Rosiglitazone and cardiovascular risk, New Eng J Med, 2007:356:2522-2524
- Risk of Cardiovascular Events and All-Cause Mortality in Patients Treated With Thiazolidinediones in a Managed-Care Population [7], © 2010 American Heart Association, Inc.
- Pioglitazone and the risk of cardiovascular events in patients with Type 2 diabetes receiving concomitant treatment with nitrates, renin–angiotensin system blockers, or insulin: results from the PROactive study (PROactive 20)[8], Journal of Diabetes, Volume 2, Issue 3, pages 212–220, September 2010
- Lincoff AM, Wolski K, Nicholls SJ, Nissen, SE, Pioglitazone and risk of cardiovascular events in patients with type 2 diabetes mellitus : A meta-analysis of randomized trials, JAMA, 2007;298:1180-1188
- Rosiglitazone no longer recommended, Lancet, 2008;372:1520
- GSK aurait tenté de dissimuler les risques d'un antidiabétique - Le Soir 14 juillet 2010
Wikimedia Foundation. 2010.
