- Méthode de wijs
-
Méthode de Wijs
Sommaire
Définition
L'indice d'iode d'un lipide est la masse de diiode (I2) (exprimée en gramme) capable de se fixer sur les insaturations (double liaison le plus souvent) des acides gras de 100 g de matière grasse en revanche l'indice d'iode en lui même ne posséde pas d'unité.
La méthode de Wijs nous permet de déterminer par expérimentation le nombre de doubles liaisons que possède un acide gras. Cela peut présenter un intérêt pour identifier un acide gras si l'on connaît d'autres de ses caractéristiques.
Principe
Dans cette méthode, on utilise le réactif de Wijs qui est une solution de monochlorure d'iode ICI, composé plus réactif que le diiode, mais strictement équivalent à celui-ci du point de vue du nombre de moles fixées sur les doubles liaisons. On fait alors agir le réactif de Wijs, que l'on met en excès connu, sur un corps gras non saturé, ICI se fixe sur les doubles liaisons;
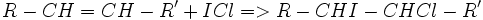
L'excès de réactif reste en solution, on ajoute alors de l'iodure de potassium en fort excès (ce composé sert également à solubiliser le diiode libéré) qui se combine à ICI en libérant du diiode.
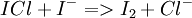
Ainsi le diiode libéré est dosé par une solution de concentration molaire connue de thiosulfate de sodium, en présence d'empois d'amidon, ajouté en fin de dosage.
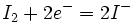
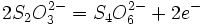
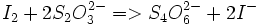
On réalise un dosage témoin dans les mêmes conditions, mais sans corps gras, afin de pouvoir déterminer la quantité de diiode qui a saturé les doubles liaisons. Il faut utiliser du matériel sec car ICl est détruit par l'eau.
Schéma du dosage
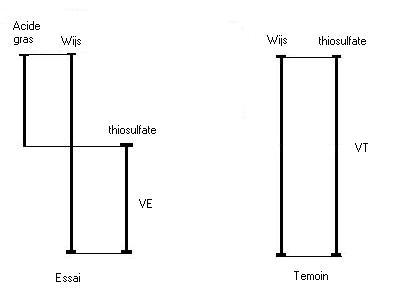
VT correspond au volume de
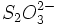 versé au témoin.
versé au témoin.VE correspond au volume de
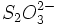 versé a l’essai.
versé a l’essai.Une masse d'acide gras est mis en excès avec du réactif de Wijs. L'excès est dosé par une solution de thiosulfate (VE). En parallèle, un témoin est réalisé dans les mêmes conditions (même réactif mais sans corps gras)
Protocole
Matériel
-
- Deux erlenmeyers avec bouchon adaptable ;
- Une pipette jaugé de 20 mL ;
- Une burette.
Solutions
-
- Du cyclohexane ;
- Du réactif de wijs ;
- De l'eau distillée ;
- De l'iodure de potassium a 100 g.L-1 ;
- Du thiosulfate de sodium a concentration de 0,2 mol.L-1 environ.
Étapes
- Dans l'erlenmeyer, introduire :
- Une masse de corps gras exactement pesée proche de 0,2 g ;
- 20 mL de cyclohexane ;
- 20 mL de réactif de Wijs ;
- Boucher et agiter energiquement.
- Laisser reposer 40 minutes à l'obscurité en secouant de temps en temps.
- Ajouter ensuite :
- 100 mL d'eau distillée ;
- 20 mL d'iodure de potassium à 100 g.L-1 ;
- Boucher et agiter vigoureusement pendant 5 minutes ;
- Doser l'iode formé par le thiosulfate de sodium.
Réaliser dans les mêmes conditions un témoin en utilisant la moitié des réactifs mais sans corps gras.
Précisions
- Les lipides sont solubles dans les solvants organiques et non dans l'eau d'où l'utilisation de cyclohexane.
- Le diiode est plus soluble dans le cyclohexane que dans l'eau, c'est pour cela qu'il faut agiter pour faire passer le diiode dans l'eau, là où il peut être dosé.
- Quand la phase aqueuse est presque décolorée, ajouter 1 mL d'empois d'amidon puis continuer le dosage jusqu'a décoloration totale des deux phases.
- La réalisation d'un témoin est nécessaire pour la réalisation des calculs. Le témoin peut être fait avec la moitié ou la totalité des réactifs
- Ne jetez rien dans le lavabo ! Débarrassez-vous des déchets organiques dans un conteneur prévu à cet effet.
Calculs
Détermination de l'indice d'iode
(si vous avez fait un témoin avec tous les réactifs ne multipliez pas VT par 2)
Une mole de
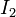 réagit avec 2 moles de
réagit avec 2 moles de 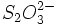 , donc :
, donc :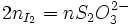
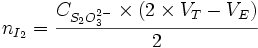
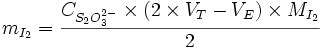
Ensuite, il faut rapporter à 100 g de corps gras.
Exemple :
- 0,155 g de I2 réagissent avec 0.183 g de corps gras.
- x g de I2 réagissent avec 100 g de corps gras.
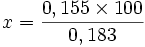
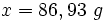
Détermination du nombre de double liaisons
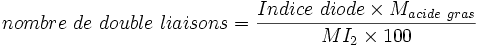
Quelques Indices d'iode
indice diode de Corps Gras Végetaux Coprah 5-9 Palmiste 12-19 Palme 45-58 Olive 83-87 Arachide 90-98 Maïs 110-128 Tournesol 120-136 Soja 125-138 Noix 135-150 Lin cultivé 170-202 Colza 97-107 indice diode de Corps Gras Animaux Beurre 30-45 Suif de bœuf 42-48 Saindoux 52-68 Hareng 135-140 Sardine 170-190 Baleine 105-120 Voir aussi
- Portail de la chimie
Catégories : Technique de laboratoire | Chimie analytique | Lipide -
Wikimedia Foundation. 2010.
