- Iodure de propidium
-
Iodure de propidium 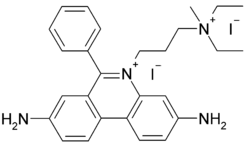
Général Nom IUPAC diiodure de 3,8-diamino-5-[3-(diéthylméthylammonio)propyl]-6-phénylphénantridinium No CAS No EINECS PubChem SMILES InChI Apparence solide: rouge sombre;
en solution: rouge foncé
à orange selon la concentration.Propriétés chimiques Formule brute C27H34I2N4 [Isomères] Masse molaire[1] 668,3946 ± 0,0248 g·mol-1
C 48,52 %, H 5,13 %, I 37,97 %, N 8,38 %,Propriétés physiques T° fusion 210 à 230 °C (décomposition)[2] Propriétés optiques Fluorescence λexcitation 305 nm et 538 nm;
λémission 617 nmPrécautions Directive 67/548/EEC[3] 
XiPhrases R : 36/37/38, Phrases S : 26, Écotoxicologie DL50 16 mg·kg-1 (souris, s.c.)[4] Unités du SI & CNTP, sauf indication contraire. L'iodure de propidium (IP ou PI pour propidium iodide) est un agent intercalant des acides nucléiques (l'ADN ou l'ARN) et une molécule fluorescente ayant une masse moléculaire de 668,403 Da. L'IP est couramment utilisé comme marqueur de l'ADN afin de marquer le noyau des cellules ayant perdu leur intégrité membranaire (phénomène caractéristique de la nécrose).
Sommaire
Utilisation en biologie moléculaire
A l'instar du bromure d'éthidium (BEt), l'iodure de propidium (IP) est un agent d'intercalation utilisé comme marqueur des acides nucléiques. Il se lie aux bases de l'ADN avec peu ou pas de spécificité de séquence et suivant une stœchiométrie d'une molécule pour 4-5 paires de bases. L'IP peut aussi se lier à l'ARN[5] et c'est pour cela qu'un traitement à l'aide de nucléases (RNases) s'avère nécessaire afin de dégrader l'ARN et d'éviter ainsi tous faux positifs. Par ailleurs, une molécule d'IP se liant aux acides nucléiques est 20 à 30 fois plus fluorescente qu'une molécule libre en solution, le maximum d'excitation étant décalé d'environ 30 à 40 nm vers le rouge et le maximum d'émission décalé d'environ 15 nm vers le bleu. L'IP est utilisé en imagerie cellulaire (microscopie à fluorescence, microscopie confocale), en cytométrie en flux[6] ou encore en fluorométrie.
Son utilisation principalement en imagerie cellulaire et en cytométrie en flux s'explique par sa relative lipophobie. En effet, contrairement au bromure d'éthidium qui a la capacité de traverser relativement facilement les membranes plasmiques, l'IP par son second ammonium quaternaire possède une lipophobie (ou hydrophilie) relativement plus élevée. Ceci fait de lui un puissant marqueur de la viabilité cellulaire : en effet, une cellule viable possède une intégrité membranaire, l'IP ne pouvant alors pénétrer et se lier à l'ADN présent dans la cellule, au contraire d'une cellule morte dont la membrane perméabilisée pourra laisser entrer l'IP qui se liera à l'ADN. Par ailleurs, l'IP peut être utilisé en parallèle d'autres marqueurs fluorescents (techniques du multimarquage). Ainsi l'IP est compatible avec des marquages directs ou indirects par anticorps, avec des marquages en hybridation in situ ou bien encore avec des marquages utilisant des fluorophores spécifiques de structures cellulaires.
Détection des phénomènes de nécrose et d'apoptose
En cytométrie en flux, l'IP permet de distinguer facilement les cellules vivantes des cellules mortes. Mais il est possible de distinguer dans les populations de cellules mortes, les sous-populations de cellules nécrotiques et de cellules apoptiques[7]. Pour cela, il est nécessaire de réaliser un double marquage à l'aide d'un second fluorophore : une annexine fusionnée à la GFP. Ce marquage se base sur un phénomène caractéristique ayant lieu au sein des cellules apoptotiques : l'inversion des feuillets lipidiques de la membrane cytoplasmique. Cette inversion entraîne l'exposition vers le milieu extérieur de phospholipides modifiés habituellement absents, parmi lesquels les phosphatidylsérines. Or les annexines sont une famille de molécules impliquée dans la signalisation cellulaire et ayant la capacité de se fixer à ces phosphatidylsérines. Ainsi, en utilisant une annexine fusionnée à la GFP, il est possible de distinguer les cellules apoptiques (marquées seulement à l'annexine5) des cellules nécrotiques (marquées avec l'annexine et marquées avec l'IP).
Détection des parois cellulaires chez les végétaux
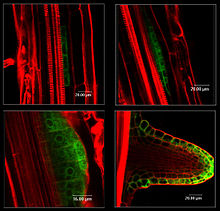 Fig 1. Image en microscopie à fluorescence de la croissance de primordia racinaires ches Arabidopsis thaliana. Les primordia sont marquées par la GFP (vert), la paroi cellulaire par l'IP (rouge)
Fig 1. Image en microscopie à fluorescence de la croissance de primordia racinaires ches Arabidopsis thaliana. Les primordia sont marquées par la GFP (vert), la paroi cellulaire par l'IP (rouge)
Une des applications de l'IP en biologie végétale concerne le marquage des parois cellulaires. En effet, il est possible d'observer, suite au marquage à l'IP, le contour des cellules, l'IP restant autour des cellules au sein de la paroi du tissu végétale observée. On peut ainsi par exemple observer en microscopie confocale le contour des cellules du tissu racinaire des graines d'Arabidopsis thaliana. Il est alors possible de localiser avec précision dans quelle partie de la racine peut s'exprimer un gène d'intérêt si ce dernier a été fusionné avec le gène codant la GFP.
Sécurité et effets sur la santé
Bien qu'aucune fiche n'ait encore été édité par l'INRS à propos de l'IP, il s'agit d'un produit nocif[8]. Il doit être manipulé avec précaution et bien que sa relative lipophobie limite sa pénétration rapide dans les tissus, l'usage de gants en latex voire en nitrile est indispensable.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) W.L.F. Armarego, Christina Chai, Purification of Laboratory Chemicals, Butterworth-Heinemann Ltd, 2009, 6e éd., 760 p. (ISBN 1856175677) [lire en ligne (page consultée le 6 novembre 2009)], p. 423
- (de) Gudrun Lang, Histotechnik: Praxislehrbuch Fur Die Biomedizinische Analytik, Springer Verlag GmbH, 2006, 427 p. (ISBN 3211331417) [lire en ligne (page consultée le 6 novembre 2009)], p. 402
- British Journal of Pharmacology and Chemotherapy. Vol. 11, p 334, 1956.
- (en) Suzuki T, Fujikura K, Higashiyama T, Takata K, « DNA staining for fluorescence and laser confocal microscopy », dans J. Histochem. Cytochem., vol. 45, no 1, 1997, p. 49–53 [texte intégral] PMID 9010468
- (en) Lecoeur H, « Nuclear apoptosis detection by flow cytometry: influence of endogenous endonucleases », dans Exp. Cell Res., vol. 277, no 1, 2002, p. 1–14 [lien DOI] PMID 12061813
- (en) Moore A, Donahue CJ, Bauer KD, Mather JP, « Simultaneous measurement of cell cycle and apoptotic cell death », dans Methods Cell Biol., vol. 57, 1998, p. 265–78 PMID 9648110
- Le risque chimique
Références
Voir aussi
Liens externes
- Portail de la chimie
- Portail de la biologie cellulaire et moléculaire
Catégories :- Produit chimique irritant
- Marqueur fluorescent
- Quinoléine
- Ammonium quaternaire
- Aminobenzène
- Azine
Wikimedia Foundation. 2010.

