- Dissection Aortique
-
Dissection aortique
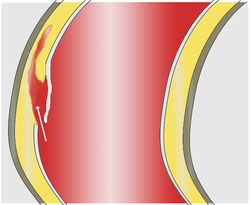
Dissection aortique CIM-10 : I71 La dissection aortique est une affection rare et grave caractérisée par l'irruption de sang à l'intérieur de la paroi de l'aorte. Il se constitue une déchirure ou porte d'entrée, par laquelle le sang sous pression entre et décolle les feuillets superposées qui constituent la paroi élastique de l'aorte. La dissection de ces feuillets peut s'étendre sur une longue portion de l'aorte ascendante, la crosse et ou l'aorte descendante. Elle constitue une urgence chirurgicale lorsqu'elle intéresse l'aorte proximale.
On utilise parfois le terme d'anévrisme disséquant.
Sommaire
Épidémiologie
Son incidence annuelle est d'environ 3 cas pour 100 000 personnes[1].
La mortalité en est élevée puisque près de la moitié des patients décèdent à la phase aiguë (20% avant l'arrivée à l'hôpital)[2].
Mécanisme
Voir l'article aorte pour un rappel anatomique.Le terrain essentiel de la dissection est la présence d'une hypertension artérielle non stabilisée sous traitement. Elle peut survenir également chez des patients porteurs de maladie de la fibre élastique (contenus notamment dans l'aorte) comme la maladie de Marfan. La préexistence d'un anévrisme aortique est décrite dans un cinquième des cas[1].
La formation d'un hématome (collection de sang coagulé) de paroi aortique est une entité décrite depuis la fin des années 90 et peut évoluer vers la dissection. Il n'est pas sûr que cela soit le seul mécanisme responsable mais la découverte d'une telle anomalie peut imposer un traitement chirurgical rapide.
La dissection débute par une porte d'entrée, rupture de la paroi interne (intima) permettant le décollement de cette dernière en pleine media (partie moyenne de la paroi). Ce décollement s'étend le plus souvent d'amont en aval et forme un poche de sang circulant, le faux chenal, séparé du vrai chenal (la lumière de l'artère) par un flap (constitué par la paroi décollée). Plus rarement, la progression se fait en rétrograde (d'aval en amont).
C'est une affection gravissime car elle peut progresser rapidement et provoquer en amont :
- une insuffisance de la valve aortique massive par basculement d'une cuspide de cette dernière, entraînant une insuffisance cardiaque grave ;
- la rupture dans le péricarde entraînant un épanchement péricarditique sanguin abondant avec compression du cœur (tamponnade) pouvant évoluer vers une défaillance cardiaque et un arrêt cardio-circulatoire ;
- une dissection par extension des artères coronaires avec occlusion de ces dernières et constitution d'un infarctus du myocarde;
en aval :
- une rupture de l'aorte avec hémorragie interne massive fatale ;
- une progression de la dissection sur les différentes artères avec occlusion des ces dernières (ou baisse importante de leur débit) donnant un tableau d'ischémie localisé (accident vasculaire cérébral s'il s'agit d'une artère à destinée encéphalique, infarctus rénal s'il s'agit d'une artère rénale…).
En pratique, les complications les plus graves sont celles concernant le cœur et n'arrive que si la dissection concerne l'aorte ascendante. Cette dernière constitue donc une urgence chirurgicale absolue. Les dissections de l'aorte descendante doivent être dans un premier temps traitées médicalement (par médicaments) et la chirurgie se discute alors cas par cas.
Classification
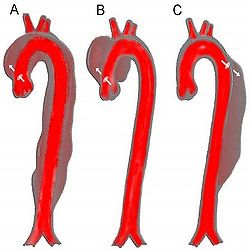
La classification de DeBakey est une classification anatomique des dissections de l'aorte en fonction de l'origine de la dissection et sur son extension vers l'aval. (notamment l'extension de la dissection vers l'aorte ascendante, vers la crosse ou vers l'aorte descendante).
- Type I - Débute à l'aorte ascendante, jusqu'à la crosse de l'aorte et la portion descendante. (A sur le dessin)
- Type II – Débute et se localise uniquement à l'aorte ascendante. (B sur le dessin)
- Type III – Débute et se localise à l'aorte descendante. (C sur le dessin)
De manière pratique, on distingue :
- les dissections intéressant l'aorte ascendante, constituant une urgence chirurgicale et nécessitant le transfert rapide du patient vers un centre disposant d'une chirurgie cardiaque,
- les dissections intéressant uniquement l'aorte descendante, dont le traitement reste essentiellement médicamenteux (baisse de la pression artérielle) même si elle requiert, plus rarement, une chirurgie.
Diagnostic
Le diagnostic a longtemps reposé sur l'angiographie. Cependant, cette méthode a été supplantée par l'avènement de l'échographie transœsophagienne, pouvant être faite au lit du patient et du scanner thoracique. L'imagerie par résonance magnétique permet également d'en faire le diagnostic.
Lors de douleurs retrosternales, on effectue systématiquement un ECG pour déceler un éventuel infarctus.
Clinique
La dissection aortique est une affection brutale dominée par la douleur thoracique. Cette dernière se caractérise par son caractère migrateur (sa position varie dans le temps). La douleur peut être absente dans un cas sur 10[3].
On recherche systématiquement un terrain favorisant : hypertension artérielle, syndrome de Marfan (se caractérisant principalement par une grande taille, avec de long bras et doigts, une déformation du thorax, parfois enfoncé, une souplesse articulaire importante témoignant d'une hyperlaxité des ligaments).
L'examen clinique recherche :
- une abolition d'un ou plusieurs pouls, pouvant témoigner de l'extension de la dissection sur une artère périphérique ;
- un souffle à l'auscultation cardiaque, témoin d'une insuffisance de la valve aortique par atteinte de ses cuspides ;
- une pression artérielle différente aux deux bras (asymétrie tensionnelle) témoignant de la dissection de l'origine de l'une des artères à destination des membres supérieurs ;
- des signes de mauvaise tolérance (collapsus cardio-vasculaire, voire arrêt cardio-circulatoire).
Suivant le niveau et l'extension de la dissection, le patient peut présenter des signes
- d'un infarctus du myocarde par atteinte d'une artère coronaire ;
- d'un accident vasculaire cérébral par atteinte d'une carotide ou d'une artère vertébrale ;
- d'une ischémie aiguë du membre inférieur par atteinte d'une artère fémorale ;
- d'une tamponnade par compression du cœur par un épanchement de sang dans le péricarde.
La rupture de l'aorte entraîne un décès rapide et ne pose donc guère de problème diagnostic.
Dès la suspicion de dissection, le patient doit être admis rapidement, et de manière médicalisé, dans un centre pouvant confirmer le diagnostic avant un éventuel transfert en chirurgie cardiaque.
Examens complémentaires
Plusieurs examens permettent le diagnostic. Le choix de l'un ou l'autre dépend essentiellement de la disponibilité des appareils et du médecin l'effectuant en urgences.
- Le scanner thoracique avec injection de produit de contraste dans le système vasculaire montre un double contraste de l'aorte qui est coupée en deux par le flap. Il permet de bien en délimiter l'extension.
- L'échographie transœsophagienne consiste à faire avaler au patient, sous anesthésie locale, une sonde d'échographie fixé à un endoscope. L'examen permet de bien visualiser la quasi intégralité de l'aorte thoracique. En cas de dissection, le flap est clairement objectivé, ainsi que, parfois, la porte d'entrée et/ou de sortie. L'insuffisance de la valve aortique et son mécanisme peuvent être, également, facilement évalués. L'extension de la dissection vers l'aorte abdominale ne peut être analysée par cette technique, mais cette donnée reste secondaire dans la conduite à tenir (cf. classification des dissections).
- La radiographie de thorax montre une modification de la silhouette de l'aorte (élargissement du médiastin).
- L'électrocardiogramme (ECG) peut montrer les signes d'une hypertrophie ventriculaire gauche secondaire à une hypertension non ou mal soignée. Il peut montrer également les signes d'un infarctus en cours de constitution. Le plus souvent, l'ECG est normal.
L'échocardiographie "classique", dite trans-thoracique ne suffit pas à elle seule, à éliminer le diagnostic de dissection, l'aorte thoracique étant une structure relativement profonde, mal visualisée par cette technique.
De même, l'artériographie avec injection de produit de contraste intravasculaire est une technique abandonnée de nos jours, car la montée d'une sonde dans une artère disséquée peut aggraver la dissection.
Dans tout les cas, on effectue un bilan biologique pré-opératoire :
- Ionogramme sanguin avec dosage de la créatinine pour évaluer la fonction rénale ;
- Numération formule sanguine ;
- recherche d'une anomalie de la coagulation par la mesure du temps de céphaline activé et du taux de prothrombine ;
- recherche du groupe sanguin et du groupe Rhésus, recherche d'agglutinines irrégulières pour une éventuelle transfusion.
- Le dosage des D-dimères sanguins (produits de dégradation de la fibrine) est, en règle, à un taux élevé, à tel point qu'un dosage normal pourrait permettre d'éliminer le diagnostic de dissection[4].
Forme clinique : l'hématome de paroi
Appelé également « hématome intra mural », il consiste en une collection de sang dans la paroi aortique, sans flap visible. Il évolue dans plus d'un quart des cas vers une dissection classique[5].
Cliniquement, il n' y a habituellement pas d'asymétrie de la pression artérielle entre les deux bras et pas de signe d'ischémie.
Il est diagnostiqué lors d'un scanner ou lors d'une échographie transœsophagienne.
Sa prise en charge est calquée sur celle de la dissection classique : chirurgie urgente s'il concerne l'aorte thoracique ascendante, traitement médicamenteux s'il concerne l'aorte descendante.
Traitement
Historique du traitement
La première intervention, décrite en 1935 consistait à effectuer une brèche (fenestration) dans la paroi du faux chenal, permettant ainsi une issue de secours pour le sang vers le vrai chenal et diminuant la pression dans le faux chenal[6]. A la fin des années 1940, on tentait de renforcer l'aorte disséquée en la doublant d'un tissu de cellophane[7].
Ce n'est qu'en 1955 que le Dr. Debakey décrit l'intervention qui a toujours lieu, consistant en la pose d'une prothèse dans l'aorte ascendante[8].
L'intérêt d'une baisse de la pression artérielle n'a été décrite que tardivement (milieu des années 1960)[9].
Traitement médical
Une hospitalisation urgente en milieu spécialisé est nécessaire.
Dans tous les cas, le traitement médical vise à faire baisser au maximum la pression artérielle et de manière rapide, avec un traitement intra-veineux.
Traitement chirurgical
En cas de dissection de l'aorte thoracique ascendante, le traitement est une urgence chirurgicale. Cela nécessite le transfert dans un centre de chirurgie cardiaque, la mise en place d'une circulation extra-corporelle étant nécessaire. L'intervention consiste, après ouverture verticale du sternum (sternotomie médiane), en la mise en place d'un tube dans l'aorte ascendante avec fermeture des portes d'entrée et de sortie. Suivant l'extension, le geste peut être associé à un remplacement de la valve aortique ou à une simple remise en place des cusps aortiques, à une réimplantation des artères coronaires ou des autres vaisseaux dans le tube.
En cas de dissection isolée de l'aorte abdominale, le traitement est essentiellement médicamenteux pour assurer un contrôle de la pression artérielle optimal. L'évolution n'en est pas pour autant bénigne, avec un risque de décès augmenté[10]
Traitement par cathétérisme
La mise en place d'une endo-prothèse (ou stent, « endo » signifiant que la prothèse est située à l'intérieur du vaisseau, ne remplaçant donc pas ce dernier) au cours d'un simple cathétérisme (par voie fémorale, et donc, sans chirurgie ni circulation extra-corporelle) est une technique alternative de traitement des anévrismes de l'aorte.
Cette méthode a été utilisée également au cours de dissections aortiques, le stent permettant l'écrasement du faux chenal et facilitant ainsi son occlusion, soit par simple effet mécanique, soit par fermeture d'une porte d'entrée. Cette technique reste encore en cours d'évaluation[11].
Notes et références
- ↑ a et b Golledge J, Eagle KA, Acute aortic dissection, Lancet, 2008;372:55-66
- ↑ Olsson C, Thelin S, Stahle E, Ekbom A, Granath F, Thoracic aortic aneurysm and dissection: increasing prevalence and improved outcomes reported in a nationwide population-based study of more than 14000 cases from 1987 to 2002, Circulation, 2006;114:2611-2618
- ↑ Hagan PG, Nienaber CA, Isselbacher EM, et als. The International Registry of Acute Aortic Dissection (IRAD): new insights into an old disease, JAMA, 2000;283:897-903
- ↑ Toru Suzuki, Distante A, Zizza A et Als. Diagnosis of acute aortic dissection by D-Dimer: The International Registry of Acute Aortic Dissection Substudy on Biomarkers (IRAD-Bio) Experience, Circulation, 2009;119:2702-2707
- ↑ von Kodolitsch Y, Csösz SK, Koschyk DH et als. Intramural hematoma of the aorta: predictors of progression to dissection and rupture, Circulation, 2003;107:1158–63
- ↑ Gurin D, Bulmer JW, Derby R, Dissecting aneurysms of the aorta: diagnosis and operative relief of arterial obstruction due to this cause, N Y State J Med, 1935;35:1200
- ↑ Abbott OA, Clinical experiences with application of polythene cellophane upon aneurysms of thoracic vessels, J Thorac Surg, 1949;18:435
- ↑ DeBakey ME, Cooley DA, Creech O Jr, Surgical considerations of dissecting aneurysm of the aorta, Ann Surg, 1955;142:586–610
- ↑ Wheat MW Jr, Palmer RF, Bartley TD, Seelman RC, Treatment of dissecting aneurysms of the aorta without surgery, J Thorac Cardiovasc Surg. 1965;50:364–373
- ↑ (en)Long-term survival in patients presenting with type B acute aortic dissection , Thomas T. Tsai, Rossella Fattori, Santi Trimarchi, Eric Isselbacher, Truls Myrmel, Arturo Evangelista, Stuart Hutchison, Udo Sechtem, Jeanna V. Cooper, Dean E. Smith, Linda Pape, James Froehlich, Arun Raghupathy, James L. Januzzi, MD; Kim A. Eagle, Christoph A. Nienaber, Circulation, 2006;114:2226-2231.
- ↑ Swee W, Dake MD, Endovascular management of thoracic dissections, Circulation, 2008;117:1460-1473
Voir aussi
Liens internes
- Portail de la médecine
Catégories : Maladie cardio-vasculaire | Chirurgie
Wikimedia Foundation. 2010.