Acide sulfureux
- Acide sulfureux
-
| Acide sulfureux |
|
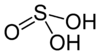 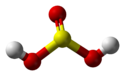

Structure de l'acide sulfureux. |
| Général |
| Nom IUPAC |
acide sulfureux
sulfite d'hydrogène |
| No CAS |
7782-99-2 |
| No EINECS |
231-973-1 |
| PubChem |
1100 |
| SMILES |
|
| InChI |
InChI : Vue 3D
InChI=1S/H2O3S/c1-4(2)3/h(H2,1,2,3)
InChIKey :
LSNNMFCWUKXFEE-UHFFFAOYSA-N
|
| Propriétés chimiques |
| Formule brute |
H2O3SH2SO3 |
| Masse molaire[1] |
82,079 ± 0,006 g·mol-1
H 2,46 %, O 58,48 %, S 39,07 %,
|
| pKa |
1,81 et 6,99 |
| Propriétés physiques |
| Solubilité |
Miscible à l'eau [2] |
| Masse volumique |
1,03 g·cm-3 (20 °C)[2] |
| Précautions |
|
Directive 67/548/EEC[2]
|

C
|
|
Symboles :
C : Corrosif
Phrases R :
R20 : Nocif par inhalation.
R34 : Provoque des brûlures.
Phrases S :
S26 : En cas de contact avec les yeux, laver immédiatement et abondamment avec de l’eau et consulter un spécialiste.
S45 : En cas d’accident ou de malaise, consulter immédiatement un médecin (si possible, lui montrer l’étiquette).
S36/37/39 : Porter un vêtement de protection approprié, des gants et un appareil de protection des yeux/du visage.
|
| Phrases R : 20, 34, |
| Phrases S : 26, 36/37/39, 45, |
|
Transport[2]
|
Code Kemler :
80 : matière corrosive ou présentant un degré mineur de corrosivité
Numéro ONU :
1833 : ACIDE SULFUREUX
Classe :
8
Étiquette :
 8
8 : Matières corrosives
Emballage :
Groupe d'emballage II : matières moyennement dangereuses;
|
|
SIMDUT[3]
|
 E,
E,
E : Matière corrosive
Transport des marchandises dangereuses : classe 8
Divulgation à 1,0% selon la liste de divulgation des ingrédients
|
|
SGH[4]
|
 H314, H332, P280, P305, P310, P338, P351,
H314, H332, P280, P305, P310, P338, P351,
H314 : Provoque de graves brûlures de la peau et des lésions oculaires
H332 : Nocif par inhalation
P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage.
P305 : EN CAS DE CONTACT AVEC LES YEUX:
P310 : Appeler immédiatement un CENTRE ANTIPOISON ou un médecin.
P338 : Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer.
P351 : Rincer avec précaution à l’eau pendant plusieurs minutes.
|
|
Unités du SI & CNTP, sauf indication contraire.
|
L’acide sulfureux est un composé chimique de formule H2SO3. S'il a été détecté en phase gazeuse[5], il n'est en revanche pas certain qu'il existe effectivement en solution.
Les bases conjuguées de cet acide sont quant à elles communes : l'anion hydrogénosulfite de formule HSO3- et l'anion sulfite de formule SO32-.
Description
L'acide sulfureux est un acide minéral résultant formellement de la dissolution de dioxyde de soufre SO2 dans de l'eau H2O selon la réaction :
- SO2 (g) + H2O(l) → H2SO3 (aq) : K << 10-9.
Cependant, la molécule H2SO3 solvatée par l'eau n'est pas stable et conduit immédiatement aux ions hydrogénosulfite HSO3- et sulfite SO32- :
- SO2 (g) + 2 H2O(l)
 H3O+(aq) + HSO3-(aq) : pKa1 = 1,81.
H3O+(aq) + HSO3-(aq) : pKa1 = 1,81.
- HSO3-(aq) + H2O(l)
 H3O+(aq) + SO32-(aq) : pKa2 = 6,99.
H3O+(aq) + SO32-(aq) : pKa2 = 6,99.
Ce type de solution acide est utilisé comme conservateur alimentaire, notamment pour les fruits secs, le vin et la conservation de la viande, ainsi que comme désinfectant, agent réducteur et blanchissant doux, utilisé notamment sur les matériaux qui seraient endommagés par un blanchissage aux produits chlorés.
Notes et références
- ↑ Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- ↑ a, b, c et d Entrée de « Sulfurous acid » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 27 novembre 2009 (JavaScript nécessaire)
- ↑ « Acide sulfureux » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ SIGMA ALDRICH
- ↑ D. Sülzle, M. Verhoeven, J. K. Terlouw, H. Schwarz, "Preparation and characterization of sulfurous acid and its radical cation as stable molecules in the gas phase" Angew. Chem. Int. Edn. Engl. 27, 1533-4 (1988). DOI:10.1002/ange.1988100112
Articles connexes
Wikimedia Foundation.
2010.
Contenu soumis à la licence CC-BY-SA. Source : Article Acide sulfureux de Wikipédia en français (auteurs)
Regardez d'autres dictionnaires:
Acide Sulfureux — Général Nom IUPAC Acide sulfureux No CAS … Wikipédia en Français
Acide sulfureux — ● Acide sulfureux acide H2SO3, non isolé mais existant en solution … Encyclopédie Universelle
sulfureux — sulfureux, euse [ sylfyrø, øz ] adj. • 1549; sulphureux XIIIe; lat. sulfurosus 1 ♦ Qui contient du soufre libre ou à l état d ion sulfure; qui est relatif au soufre. Vapeurs, exhalaisons sulfureuses. « Le rayon sulfureux qu en des songes funèbres … Encyclopédie Universelle
sulfureux — sulfureux, euse (sul fu reû, reû z ) adj. 1° Qui tient de la nature du soufre. • Des exhalaisons sulfureuses et minérales, RAYNAL Hist. phil. VI, 19. • Ce reflet émané du corps de Lucifer, C était le pâle jour qu il traîne en nos ténèbres,… … Dictionnaire de la Langue Française d'Émile Littré
acide — [ asid ] adj. et n. m. • 1545; lat. acidus I ♦ Adj. 1 ♦ Qui est piquant au goût. ⇒ aigre. Une saveur un peu acide. ⇒ acidulé. L oseille est acide. Fruit encore vert et acide. ⇒ 2. sur. ♢ Fig. Acerbe, désagréable. Des propos, des réflexions acides … Encyclopédie Universelle
Acide Faible — Sommaire 1 Définition 2 Exemples d acides faibles 2.1 Acides organiques 2.2 Acides minéraux 3 … Wikipédia en Français
Acide Sulfonique — Structure de l acide sulfonique L acide sulfonique est un acide hypothétique de formule chimique HSO2OH. C est un tautomère instable de l acide sulfureux HO SO OH. Du fait de son instabilité, c est un composé qui présente peu d intérêt en lui… … Wikipédia en Français
Acide disulfureux — Molécule d acide disulfureux Général PubChem … Wikipédia en Français
Acide chlorosulfureux — ● Acide chlorosulfureux acide HSO2Cl, premier chlorure de l acide sulfureux … Encyclopédie Universelle
SULFUREUX — EUSE. adj. Qui tient de la nature du soufre. Matière sulfureuse. Exhalaisons sulfureuses. Eaux sulfureuses. En Chimie, Acide sulfureux, Acide dont l odeur est piquante, et qui se forme par la combustion du soufre dans l air. C est à l acide… … Dictionnaire de l'Academie Francaise, 7eme edition (1835)






 H3O+(aq) + HSO3-(aq) : pKa1 = 1,81.
H3O+(aq) + HSO3-(aq) : pKa1 = 1,81. H3O+(aq) + SO32-(aq) : pKa2 = 6,99.
H3O+(aq) + SO32-(aq) : pKa2 = 6,99.
