- C13H9N
-
Acridine
Acridine 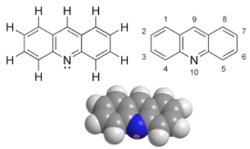
Structure de l'acridine Général Nom IUPAC Acridine Synonymes 9-azaanthracène, benzo[b]quinoléine No CAS No EINECS SMILES InChI Apparence Solide blanc Propriétés chimiques Formule brute C13H9N [Isomères] Masse molaire 179,2173 g∙mol-1
C 87,12 %, H 5,06 %, N 7,82 %,pKa 5,6 Propriétés physiques T° fusion 107 °C T° ébullition 346 °C Précautions Directive 67/548/EEC 
XiTransport - 2713 Unités du SI & CNTP, sauf indication contraire. L'acridine, de formule chimique C13H9N, est un hétérocycle azoté. Le nom désigne aussi les composés contenants le cycle triple C13N. Elle est apparentée structurellement à l'anthracène, dont on aurait remplacé un des groupes CH centraux par un azote. Elle a été originellement isolée de la houille.
C'est une matière première utilisée pour la production de pigments et de quelques médicaments. De nombreuses acridines, comme la proflavine, ont aussi une activité antiseptique. L'acridine et ses dérivés se lient à l'ADN et à l'ARN, grâce à leurs propriétés d'intercalation. L'acridarsine est formellement dérivée de l'acridine par le remplacement de l'atome d'azote par un atome d'arsenic, et l'acridophosphine par un atome de phosphore.
Sommaire
Historique
L'acridine a été isolée pour la première fois en 1871 par Carl Gräbe et Heinrich Caro.
Synthèse
L'acridine existe naturellement dans la houille. Elle est extraite par l'acide sulfurique dilué. L'addition de dichromate de potassium précipite le bichromate d'acridinium. Celui-ci libère l'acridine par réaction avec l'ammoniaque.
De nombreux procédés synthétiques permettent l'accès à l'acridine et à ses dérivés. Par exemple, A. Bernthsen condense la diphénylamine avec des acides carboxyliques en présence de chlorure de zinc. Avec l'acide formique, on obtient l'acridine. Avec les homologues, on obtient des dérivés substitués en position méso.
D'autres méthodes plus anciennes incluent la condensation de la diphénylamine avec le chloroforme en présence de chlorure d'aluminium, la réaction en phase gaz d'orthoaminodiphénylméthane, le chauffage d'acide salicylique avec l'aniline et le chlorure de zinc à 260 °C, ou la distillation de l'acridone en présence de zinc en poudre.
Une méthode générale est la cyclisation d'acide N-phénykanthranilique ou d'acide 2-(phénylamino)benzoïque avec l'acide phosphorique.
Propriétés physiques
L'acridine et ses homologues sont des composés stables, faiblement basiques (pKa = 5,6, comparable à la pyridine). Elle partage des propriétés avec la quinoléine. L'acridine cristallise sous forme d'aiguilles qui fondent à 110 °C. C'est un irritant de la peau. Ses sels donnent une fluorescence bleue en solution.
Propriétés chimiques
L'acridine réagit avec les halogénures d'alkyles et s'alkyle facilement sur l'azote. Ces composés s'oxydent facilement par l'action d'une base pour donner des N-alkylacridones.
L'oxydation par le permanganate de potassium donne l'acide acridinique C9H5N(COOH)2. Des réactions d'addition peuvent aussi avoir lieu assez facilement en position 9. Le composé est réduit en 9,10-dihydroacridine et la réaction avec le cyanure de potassium donne le dérivé 9-cyano-9,10-dihydro.
De nombreux dérivés de l'acridine sont connus. Ainsi, la 9-phénylacridine est la base de la chrysaniline, un pigment, produit secondaire de la fabrication de la rosaniline.
La chrysaniline forme des sels rouges, qui peuvent teindre la soie et la laine en jaune. Leurs solutions présentent une fluorescence jaune-vert. La chrisaniline a été synthétisée par O. Fisher et G. Koerner par la condensation de l'orthonitrobenzaldéhyde avec l'aniline, le composé résultant étant par la suite oxydé en chrysaniline.
La benzoflavine est un isomère de la chrysaniline, et est aussi un colorant. Elle a été préparée par K. Oehler à partir du méta-phénylènediamine et le benzaldéhyde. Après condensation de ces composés, perte d'ammoniac au chauffage et oxydation, on obtient la benzoflavine. C'est une poudre jaune, soluble dans l'eau chaude.
Sécurité
L'acridine est un cancérigène connu chez l'homme. Il cause des mutations en s'incorporant dans l'ADN, en créant de ce fait une nouvelle base sur le brin opposé. Si cette mutation apparaît dans un gène codant, cela inactive quasiment toujours la protéine.
References
- Synthesis of Acridine-based DNA Bis-intercalating Agents Gerard P. Moloney, David P. Kelly, P. Mack Molecules 2001, 6, 230-243 [1] open source
- (en) « Acridine », dans Encyclopædia Britannica, 1911 [détail de l’édition] [lire en ligne]
Liens externes
- Harper's New Monthly Magazine, vol. XLIV, no 261, February 1872, Editor's Scientific Record, Acridine: a New Anthracene Derivative (description, publiée en 1872, de la découverte de l'acridine)
- Synthesis of acridone in Organic Syntheses 19:6; Coll. Vol. 2:15 [2] from o-chlorobenzoic acid and aniline in a Goldberg reaction.
- Synthesis of 9-aminoacridine in Organic Syntheses 22:5; Coll. Vol. 3:53. [3] from N-phenylanthranilic acid.
- Portail de la pharmacie
- Portail de la chimie
Catégories : Produit chimique irritant | Alcaloïde | Acridine
Wikimedia Foundation. 2010.
