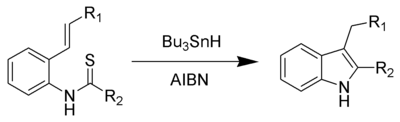
- Synthèse de Fukuyama d'indoles
-
La synthèse de Fukuyama d'indoles est une série de réactions organiques à partir d'un alkénylthioanilide pour donner des indoles 2,3-disubstitués[1]. Très souvent, le tributylétain est utilisé comme agent réducteur, avec l'AIBN comme initiateur radicalaire.
Étant l'une des méthodes les plus simples pour synthétiser les indoles poly-substitués, cette synthèse a été utilisé pour la synthèse totale de nombreux produits naturels notamment l'aspidophytine[2], la vinblastine[3] et la strychnine[4].
Notes et références
- Tokuyama, H, « Radical Cyclization of 2-Alkenylthioanilides: A Novel Synthesis of 2,3-Disubstituted Indoles », dans J. Am. Chem. Soc., vol. 121, 1999, p. 3791–3792 [lien DOI]
- Sumi, S, « Enantioselective Total Synthesis of Aspidophytine », dans Org. Lett., vol. 5, no 11, 2003, p. 1891–1893 [lien PMID, lien DOI]
- Yokoshima, S, « Stereocontrolled Total Synthesis of (+)-Vinblastine », dans J. Am. Chem. Soc., vol. 124, 2002, p. 2137–2139 [lien DOI]
- Kaburagi, Y, « Total Synthesis of (-)-Strychnine », dans J. Am. Chem. Soc., vol. 126, no 33, 2004, p. 10246–10247 [lien PMID, lien DOI]
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Fukuyama indole synthesis » (voir la liste des auteurs)
Catégories :- Réaction formant un indole
- Réaction radicalaire
Wikimedia Foundation. 2010.