- Synthèse de Bischler-Möhlau de l'indole
-
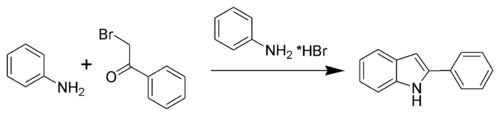
La synthèse de Bischler-Möhlau de l'indole est une réaction organique formant un 2-aryl-indole à partir d'α-bromo-acétophénone, d'aniline en excès et en présence d'acide bromhydrique[1],[2],[3],[4],[5].
Malgré sa longue histoire, cette réaction n'est plus l'objet d'attention particulière par comparaison à d'autres méthodes de synthèse d'indoles, peut-être parce que les conditions de synthèses requises sont plus rudes que dans les autres méthodes. Récemment, des méthodes plus douces ont été développés, incluant l'usage de bromure de lithium comme catalyseur, et une amélioration de la procédure impliquant une irradiation par micro-ondes[6],[7],[8].
Mécanisme réactionnel
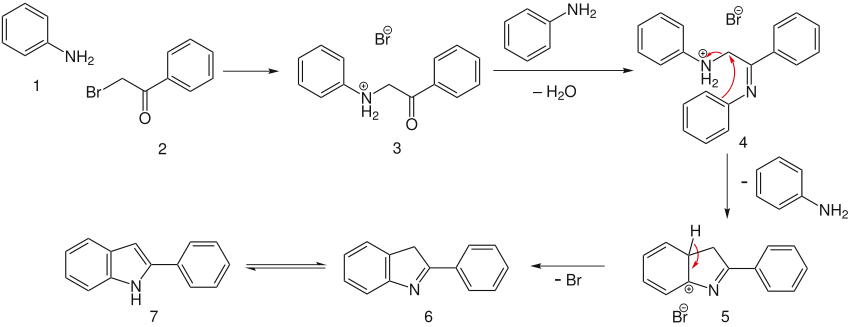
Pour une réaction avec des composés de départ initiaux aussi simple, le mécanisme réactionnel est de façon surprenante assez complexe. Les deux première étapes sont la formation par double substitution par l'aniline de l'intermédiaire réactionnel 4. À ce niveau, le noyau d'aniline chargé est un assez bon groupe partant et est éliminé par cyclisation électrophile pour former l'intermédiaire 5, qui est rapidement transformé en composé aromatique, et tautomérisé en l'indole désiré 7.
Notes et références
- Bischler, A. et al.; Ber. 1892, 25, 2860.
- Bischler, A. et al.; Ber. 1893, 26, 1336.
- Möhlau, R.; Ber. 1881, 14, 171.
- Möhlau, R.; Ber. 1882, 15, 2480.
- Fischer, E.; Schmitt, T. Ber. 1888, 21, 1071.
- Pchalek, K.; Jones, A. W.; Wekking, M. M. T.; Black, D. S. C. Tetrahedron 2005, 61, 77.
- Sridharan, V.; Perumal, S.; Avendaño, C.; Menéndez, J. C. Synlett 2006, 91.
- Vara et al 2008
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Bischler-Möhlau indole synthesis » (voir la liste des auteurs)
Voir aussi
Catégorie :- Réaction formant un indole
Wikimedia Foundation. 2010.