- Pristane
-
Pristane 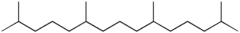
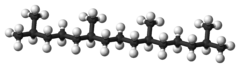
Structure du pristane, un terpène. Général Nom IUPAC 2,6,10,14-tétraméthylpentadécane Synonymes norphytane No CAS PubChem SMILES InChI Propriétés chimiques Formule brute C19H40 [Isomères] Masse molaire[1] 268,5209 ± 0,018 g·mol-1
C 84,99 %, H 15,01 %,Propriétés physiques T° fusion -100 °C[2] T° ébullition 292 à 296 °C[2] Masse volumique 0,77911 g·cm-3 à 25 °C [3] Viscosité dynamique 5,4793 Pa·s à 25 °C [3] Thermochimie Cp 569,76 J·mol-1·K-1 à 25 °C [4] Unités du SI & CNTP, sauf indication contraire.
Le pristane est un alcane terpénoide saturé naturel extrait dans un premier temps de l'huile du foie des requins, d'où son nom (en latin, pristis signifie « requin »). Il est également présent dans l'huile minérale et certains aliments[5]. Pur, il se présente sous la forme d'un liquide huileux transparent qui n'est pas miscible dans l'eau, mais est soluble dans l' éther diéthylique, le benzène, le chloroforme et le tétrachlorométhane.Le pristane est connu pour induire une réaction auto-immune chez les rongeurs. Il est utilisé dans la recherche pour comprendre la pathogénèse de la polyarthrite rhumatoïde et du lupus[6],[7]. Son utilisation dans de nombreux produits (lubrifiant, huile de transformateur, adjuvant immunologique et agent anti-corrosif) pourrait possiblement déclencher des maladies comme le lupus et la polyarthrite rhumatoïde[8].
Par chimie organique, le pristane est produit à partir de phytol.
Références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « pristane » (voir la liste des auteurs)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) J.G. Bendoraitis, B.L. Brown et L.S. Hepner, « Isoprenoid Hydrocarbons in Petroleum. Isolation of 2,6,10,14-Tetramethylpentadecane by High Temperature Gas-Liquid Chromatography », dans Analytical Chemistry, vol. 34, no 1, 1962-01-01, p. 49-53 [lien DOI (page consultée le 10 novembre)]
- (en) Maurizio Fermeglia et Giovanni Torriano, « n-C16 and Four Nonlinear Alkanes at 298.15 K », dans Journal of Chemical & Engineering Data, vol. 44, 1999-09, p. 965-969 [lien DOI (page consultée le 10 novembre 2010)]
- (en) Luis M. Trejo, Miguel Costas et Donald Patterson, « Effect of molecular size on the W-shaped excess heat capacities: oxaalkane?alkane systems », dans Journal of the Chemical Society, Faraday Transactions, vol. 87, no 18, 1991, p. 3001-3008 [lien DOI (page consultée le 10 novembre 2010)]
- (en)Chung, J. G., L. R. Garrett, P. E. Byers, and M. A. Cuchens, « A survey of the amount of pristane in common fruits and vegetables », dans J. Food Comp. Anal., vol. 2, no 22, 1989, p. 22 [lien DOI]
- (en)Anderson, P. N., and M. Potter, « Induction of plasma cell tunours in BALBfc mice with 2,6,10,14-tetramethylpentadecane (pristane) », dans Nature, vol. 222, no 5197, 1969, p. 994 [lien PMID, lien DOI]
- (en)Hazani R, Engineer N., « Surreptitious injection of mineral oil: a case report of sclerosing lipogranulomatosis », dans Ann Plast Surg, vol. 61, no 5, novembre 2008, p. 555–8 [lien PMID, lien DOI]
- (en)Frederick W Miller, « Is occupational exposure to mineral oil a risk factor for rheumatoid arthritis? », dans Nature Clinical Practice Rheumatology, vol. 2, no 3, 2006, p. 130–131 [lien PMID, lien DOI]
Wikimedia Foundation. 2010.
