- Carvacrol
-
Carvacrol 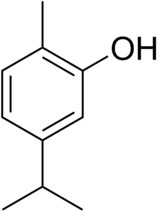
Structure du carvacrol Général Nom IUPAC 2-méthyl-5-(propan-2-yl)phénol No CAS No EINECS PubChem SMILES InChI Propriétés chimiques Formule brute C10H14O [Isomères] Masse molaire[1] 150,2176 ± 0,0093 g·mol-1
C 79,96 %, H 9,39 %, O 10,65 %,Propriétés physiques T° fusion 276,65 °C [2] T° ébullition 236,85 °C [2] Masse volumique (20 °C) 0,9772–0,98 g·cm-3 Thermochimie ΔfH0gaz -194,2 kJ·mol-1 [2] ΔfH0liquide -270 kJ·mol-1 [2] ΔvapH° 77,74 kJ·mol-1 [2] PCI -5 650 kJ·mol-1 (liquide)[2] Unités du SI & CNTP, sauf indication contraire. Le carvacrol, ou cymophénol, C6H3CH3(OH)(C3H7), est un phénol monoterpénoïde. Il a un arôme chaud et piquant, caractéristique de l'origan[3].
Sommaire
Sources naturelles
Le carvacrol se trouve dans les huiles essentielles obtenues notamment à partir de l'origan, du thym, du cresson alénois ou de la monarde. Chez le thym, l'huile essentielle contient, selon les sous-espèces, de 5 % à 75 % de carvacrol, tandis que les sous-espèces de sarriette (Satureja) en contiennent de 1 % à 45 %. Dans le genre origan, la marjolaine et le dictame de Crète sont riches en carvacrol, respectivement 50 % et 60 à 80 %[4].
Propriétés biologiques et utilisation
Le carvacrol inhibe la croissance de plusieurs souches de bactéries, par exemple Escherichia coli[5] et Bacillus cereus. Sa faible toxicité ainsi que son goût et son arôme agréables ont conduit à son utilisation comme additif alimentaire pour prévenir la contamination bactérienne[6]. Chez Pseudomonas aeruginosa, il provoque des lésions de la membrane cellulaire de ces bactéries et, contrairement à d'autres terpènes, il inhibe la prolifération de ces germes[7]. On attribue l'origine de ces propriétés antimicrobiennes à une désorganisation de la membrane bactérienne[8],[9].
C'est un activateur potentiel des potentiels récepteurs transitoires V3 (TRPV3) et A1 (TRPA1) des canaux ioniques humains[10]. L'application de carvacrol sur la langue, comme l'activation des TRPV3, provoque une sensation de chaleur. En outre, le carvacrol active, mais les désensibilise rapidement, les récepteurs de douleur TRPA1, ce qui explique son caractère piquant[10].
Chez le rat, le carvacrol est rapidement métabolisé et excrété. La principale voie métabolique est l'estérification du groupe phénolique par l'acide sulfurique et l'acide glucuronique. Une voie secondaire est l'oxydation des groupes méthyl terminaux en alcool primaires. Après un délai de 24 heures seules des traces de carvacrol ou de ses métabolites peuvent être retrouvées dans l'urine, indiquant une excrétion presque totale en un seul jour[11].
Production et synthèse
Le carvacrol peut se préparer par voie synthétique par la fusion de l'acide cymol-sulfonique avec de la potasse caustique ; par l'action de l'acide nitreux sur le 1-méthyl-2-amino-4-propyl benzène ; par le chauffage prolongé de cinq parts de camphre avec une part d'iodine ; ou par le chauffage de carvol avec glacial acide phosphorique ou en réalisant la déshydrogénation du carvone avec un catalyseur Pd/C. On peut l'extraire de l'huile d'origan par l'action d'une solution de potasse à 50 %. C'est une huile épaisse qui se prend à 20 °C en une masse de cristaux dont le point de fusion est à 0 °C, et le point d'ébullition à 236-237 °C. L'oxydation par le chlorure ferrique le convertit en dicarvacrol, tandis que pentachlorure de phosphore le transforme en chlorcymol.
Références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Carvacrol » (voir la liste des auteurs)
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) « Phenol, 2-methyl-5-(1-methylethyl)- » sur NIST/WebBook, consulté le 23 mars 2010
- (en) Ultee A, Slump RA, Steging G, Smid EJ, « Antimicrobial activity of carvacrol toward Bacillus cereus on rice », dans J. Food Prot., vol. 63, no 5, 2000, p. 620–4 [lien PMID]
- (en) De Vincenzi M, Stammati A, De Vincenzi A, Silano M, « Constituents of aromatic plants: carvacrol », dans Fitoterapia, vol. 75, no 7-8, 2004, p. 801–4 [lien PMID, lien DOI]
- (en) Du WX, Olsen CE, Avena-Bustillos RJ, McHugh TH, Levin CE, Friedman M, « Storage Stability and Antibacterial Activity against Escherichia coli O157:H7 of Carvacrol in Edible Apple Films Made by Two Different Casting Methods », dans J. Agric. Food Chem., vol. 56, 2008, p. 3082 [lien PMID, lien DOI]
- (en) Ultee A, Smid EJ, « Influence of carvacrol on growth and toxin production by Bacillus cereus », dans Int. J. Food Microbiol., vol. 64, no 3, 2001, p. 373–8 [texte intégral, lien PMID, lien DOI]
- (en) Cox SD, Markham JL, « Susceptibility and intrinsic tolerance of Pseudomonas aeruginosa to selected plant volatile compounds », dans J. Appl. Microbiol., vol. 103, no 4, 2007, p. 930–6 [lien PMID, lien DOI]
- (en) Di Pasqua R, Betts G, Hoskins N, Edwards M, Ercolini D, Mauriello G, « Membrane toxicity of antimicrobial compounds from essential oils », dans J. Agric. Food Chem., vol. 55, no 12, 2007, p. 4863–70 [lien PMID, lien DOI]
- (en) Cristani M, D'Arrigo M, Mandalari G, et al., « Interaction of four monoterpenes contained in essential oils with model membranes: implications for their antibacterial activity », dans J. Agric. Food Chem., vol. 55, no 15, 2007, p. 6300–8 [lien PMID, lien DOI]
- (en) Xu H, Delling M, Jun JC, Clapham DE, « Oregano, thyme and clove-derived flavors and skin sensitizers activate specific TRP channels », dans Nat. Neurosci., vol. 9, no 5, 2006, p. 628–35 [lien PMID, lien DOI]
- (en) Austgulen LT, Solheim E, Scheline RR, « Metabolism in rats of p-cymene derivatives: carvacrol and thymol », dans Pharmacol. Toxicol., vol. 61, no 2, 1987, p. 98–102 [lien PMID, lien DOI]
- (en) « Carvacrol », dans Encyclopædia Britannica, 1911 [détail de l’édition] [lire en ligne]
Catégories :- Monoterpène
- Phénol
- Méthylbenzène
- Cumène
Wikimedia Foundation. 2010.
