- R 22
-
Chlorodifluorométhane
Chlorodifluorométhane 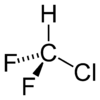
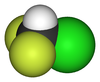
représentation du Chlorodifluorométhane Général Nom IUPAC Chlorodifluorométhane Synonymes R 22 No CAS No EINECS Apparence gaz comprimé liquefié incolore.[1] Propriétés chimiques Formule brute CHClF2 [Isomères] Masse molaire 86,468 g∙mol-1
C 13,89 %, H 1,17 %, Cl 41 %, F 43,94 %,Propriétés physiques T° fusion -146 °C[1] T° ébullition -41 °C[1] Solubilité dans l'eau à 25 °C : 0.3 g/100 ml[1] Masse volumique (eau = 1) : 1.21[1] T° d’auto-inflammation 632 °C[1] Pression de vapeur saturante à 20 °C : 908 kPa[1] Précautions Transport - 1018 SIMDUT[3] 
Classification du CIRC Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[2] Écotoxicologie LogP 1.08[1] Unités du SI & CNTP, sauf indication contraire. Le chlorodifluorométhane, CHClF2 ou R22 selon la liste des gaz fluorés et frigorigènes, est un hydrochlorofluorocarbure (HCFC). Il est aussi connu sous les appellations HCFC-22, R22, ou fréon 22, et est utilisé généralement dans des applications de climatisation. Le chlorodifluorométhane a été employé la première fois comme alternative au R11 et R12. Son potentiel d'épuisement de l'ozone est de 0,05, et figure parmi les plus bas pour les haloalkanes contenant du chlore. Toutefois, ce gaz pose un problème vis à vis du réchauffement climatique, puisqu'il a un potentiel de réchauffement global (ou PRG) 1 810 fois supérieur à celui du CO2 (tandis que le R23, sous-produit du R22, a un PRG de 14 800 fois).
Le R22 est réglementé par le protocole de Montréal, qui prévoit l'arrêt de toute consommation de HCFC dans les pays développés en 2020, et dans les pays en développement en 2040. Il est envisagé d'accélérer ces échéances, étant donné le très fort développement des HCFC, et leur très haute contribution au réchauffement climatique. En l'absence de nouvelle mesure contraignante, il est ainsi prévu que, d'ici 2015, les émissions de HCFC et de HFC représentent le double des gains engendrés en 2012 par l'application du protocole de Kyoto. De plus, l'augmentation de la demande mondiale en climatiseurs justifie la construction de nouvelles usines de production du R22, notamment en Chine, et ces nouvelles usines consomment des quantités importantes de crédits apportés par le mécanisme de développement propre prévu par le protocole de Kyoto : en effet, détruire le R23 au sein même de l'usine de production de R22 ne coûte que 0,20 US $ par tonne, pour 14 800 tonnes d'équivalent CO2 [4]
Le R22 est d'ores et déjà interdit au sein de l'Union européenne en ce qui concerne son utilisation dans les appareils neufs, depuis le 30 juin 2004. Il est encore toléré, en maintenance, sur les appareils anciens jusqu'au 1er janvier 2010. On le remplace par des réfrigérants plus respectueux de l'environnement tels que R410A (un mélange zéotropique de difluorométhane et de pentafluoroéthane), R134a (1,1,1,2-tétrafluroéthane) ou R407C.
- la lettre R signifie réfrigérant
- le chiffre des centaines représente le nombre d'atomes de carbone -1
- le chiffre des dizaines représente le nombre d'atomes d'hydrogène +1
- le chiffre des unités représente le nombre d'atomes de fluor dans la molécules
- Démonstration :
Nombre d'atomes de carbone 1⇒ 0
Nombre d'atomes d'hydrogène 1⇒ (1+1)=2
Nombre d'atomes de fluor 2⇒2
Résultat : R022
- Incolore
- Ininflammable
- Odeur : légèrement éthérée
- Ce gaz appartient a la famille des hydrochlorofluorocarbures (HCFC)
Applications industrielles
Principales applications du chlorodifluorométhane avant l'interdiction d'emploi (janvier 2015)
- Agent réfrigérant pour les installations frigorifiques
- Agent réfrigérant dans les systèmes de conditionnement d'air
- Agent de soufflage pour le polystyrène extrudé (XPS)
- Composant de mélanges stérilisant
- Le R22 sera bientôt remplacé. (Protocole de Montréal : L'accord international pour la protection de la couche d'ozone stratosphérique). En France, la fabrication de matériel l'utilisant est interdite depuis le 01/01/2004 et les appareils ne reçoivent plus le label Promotelec depuis le 01/01/2005 .
- Depuis le 1/1/2008, le R22 neuf est interdit à la vente en France. Désormais, il faudra se contenter de R134a (remplaçant le R22 car propriétés similaires) ou modifier les installations pour les faire fonctionner avec les nouveaux fluides HFC.
Propriétés
Masse molaire
- Poids moléculaire : 86,48 g/mol
Phase liquide
- Masse volumique de la phase liquide (1,013 bar au point d'ébullition) : 1 413 kg/m³
- Équivalent gaz/liquide (1,013 bar et 15 °C) : 385 vol/vol
- Point d'ébullition (1,013 bar) : -40,8 °C
- Chaleur latente de vaporisation (1,013 bar au point d'ébullition) : 233,95 kJ/kg
Point critique
- Température critique : 96 °C
- Pression critique : 49,36 bar
Phase gazeuse
- Masse volumique du gaz (1,013 bar au point d'ébullition) : 4,706 kg/m³
- Masse volumique de la phase gazeuse (1,013 bar et 15 °C) : 3,66 kg/m³
- Facteur de compressibilité (Z) (1,013 bar et 15 °C) : 0,9831
- Masse volumique (air = 1) (1,013 bar et 21 °C) : 3,08
- Volume spécifique (1,013 bar et 21 °C) : 0,275 m³/kg
- Chaleur spécifique à pression constante (Cp) (1,013 bar et 30 °C) : 0,057 kJ/(mole.K)
- Chaleur spécifique à volume constant (Cv) (1,013 bar et 30 °C) : 0,048 kJ/(mole.K)
- Rapport des chaleurs spécifiques (Gamma:Cp/Cv) (1,013 bar et 30 °C) : 1,178253
- Viscosité (1,013 bar et 0 °C) : 0,0001256 Poise
Autres données
- Solubilité dans l'eau (1 bar et 25 °C) : 0,7799 vol/vol
- ODP (Ozone Depleting Potention) : 0,05
- GWP (Golbal Warming Potential) : 1 810
Références
- ↑ a , b , c , d , e , f , g et h CHLORODIFLUOROMETHANE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme » sur http://monographs.iarc.fr, 16 janvier 2009, CIRC. Consulté le 22 août 2009
- ↑ « Monochlorodifluorométhane » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ (http://www.eia-international.org/files/reports127-1.pdf)
- Portail de la chimie
Catégories : Composé du fluor | Halogénométhane | Hydrochlorofluorocarbure | Réfrigérant
Wikimedia Foundation. 2010.
