- Pont disulfure
-
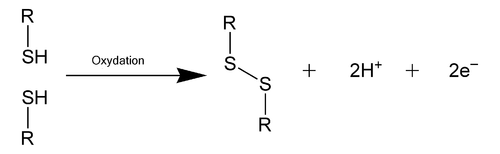
Un pont disulfure (lien S-S) est un lien covalent fort qui, par oxydation, réunit les fonctions thiol de deux cystéines dans une séquence peptidique (ou protéine) (voir la figure ci-dessous où les R représentent le reste de l'acide aminé).
La molécule résultante de la liaison de deux cystéines est la cystine.Le pont disulfure est un élément des structures tertiaires (après le repliement de la protéine) ou quaternaire (lors d'association de sous-unités protéiques) de la protéine. La formation d'un pont disulfure à partir de deux cystéines s'accomplit spontanément en conditions oxydantes, en particulier en présence de dioxygène. Ils ne se forment en général pas dans le cytoplasme, qui est un environnement réducteur, mais lorsque les protéines sont sécrétées ou exposées à la surface cellulaire.
En biochimie, la réduction d'un pont disulfure peut se faire avec des réducteurs doux, tel le 2-mercaptoéthanol ou le dithiothréitol (DTT ou réactif de Cleland).
Rôles biologiques
C'est une liaison nécessaire à la stabilisation de la structure de certaines protéines : certaines petites protéines comme les toxines présentes dans le venin de reptiles ou de scorpions ne peuvent atteindre une conformation active que parce que des ponts disulfure verrouillent leur structure.
Dans la ricine, le pont disulfure relie deux chaines A et B de fonctions complètement différentes. La chaîne B permet à la toxine de se fixer à la paroi cellulaire et la chaîne A, responsable des propriétés toxiques, est capable d’inhiber la synthèse des protéines en attaquant l'ARN des ribosomes, entraînant la mort cellulaire. La destruction du pont disulfure rend la toxine complètement inactive (elle ne peut plus pénétrer la cellule).
Dans d'autres protéines, les ponts disulfures servent à maintenir la liaison entre les différentes chaînes peptidiques ou sous-unités. C'est le cas pour les anticorps produits par les cellules du système immunitaire. Ceux-ci sont composés de quatre chaînes, deux lourdes et deux légères, reliées par des ponts disulfure. C'est également le cas de l'insuline qui est composée de deux chaînes comportant trois ponts disulfure, nécessaires à l'activité de cette hormone.
Enfin, dans quelques cas spécifiques, on trouve un pont disulfure dans le site actif de certaines enzymes ou protéines impliquées dans des processus d'oxydo-réduction ou de transport d'électron. C'est le cas par exemple des thiorédoxines qui participent à l'homéostasie de l'état redox de la cellule.
Biogénèse et localisation cellulaire
Dans les protéines contenant un grand nombre de cystéines, l'agencement correct des ponts disulfures nécessite parfois l'intervention d'une enzyme spécifique possédant une activité protéine disulfure isomérase comme la PDI (Protein disulfide isomerase). Ce processus est effectué par les protéines du réticulum endoplasmique rugueux (RER) mais pas dans le cytosol. Le cytosol des cellules est en effet un environnement très réducteur, et conséquemment les protéines cytoplasmiques contiennent donc peu ou pas de ponts disulfure. On en trouve surtout dans les protéines exportées dans d'autres compartiments cellulaires ou hors de la cellule. On en trouve également dans les domaines extracellulaires de protéines membranaires, ils interviennent en particulier dans l'oligomérisation des sous-unités de certains récepteurs comme le récepteur de l'insuline.
Dans les cheveux
Les cheveux sont constitués à 90% de kératine liées entre elles par des ponts disulfure, dont le nombre et l'emplacement donnent aux cheveux leur forme. Une permanente consiste en deux réactions chimiques successives. La première (une réduction) rompt un certain nombre de ponts disulfures. La structure de la protéine est relâchée. On enroule alors le cheveu selon la forme voulue. Cette opération amène en face les unes des autres des cystéines qui, à l'origine, étaient éloignées. La deuxième réaction (une oxydation) refait donc des ponts entre des cystéines qui ne se seraient jamais rencontrées naturellement : c'est le processus de la permanente. La protéine prend la forme ondulée imposée par la coiffeuse ou par le coiffeur.
sans oublier que les cheveux pousse pour: les chinois:2 a 3 cm /mois les français:1 a 2 cm /mois les africains:8mm a 1cm
Les réactions employées pour friser un cheveu lisse peuvent évidemment être utilisées pour étirer un cheveu frisé. Comme la destruction et la formation des ponts disulfures sont deux réactions faciles à faire; comme d'autre part, le cheveu pousse selon sa forme naturelle, la frisure ne dure qu'un temps limité.
N.B. Ceci n'est qu'une explication simplifiée de la structure du cheveu. En effet d'autres molécules sont associées à la kératine, en particulier les pigments qui donnent à chaque chevelure un éclat et une teinte unique.
Wikimedia Foundation. 2010.