Poly(styrène sulfonate) de sodium
- Poly(styrène sulfonate) de sodium
-
Poly(styrène sulfonate)
de sodium |
|
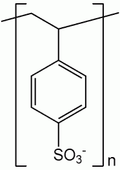
Unité de poly(styrène sulfonate)
(l'ion sodium Na+ n'est pas représenté) |
| Général |
| No CAS |
28210-41-5 |
| PubChem |
75905 |
| Apparence |
poudre blanche |
| Propriétés chimiques |
| Formule brute |
C8H7NaO3Sunité C8H7SO3Na |
| Masse molaire[1] |
206,194 ± 0,013 g·mol-1
C 46,6 %, H 3,42 %, Na 11,15 %, O 23,28 %, S 15,55 %,
|
| Propriétés physiques |
| Solubilité |
très soluble dans l'eau |
| Précautions |
|
Directive 67/548/EEC[2]
|
En solution 18 % pondéral dans l'eau :

C
|
|
Symboles :
C : Corrosif
Phrases R :
R34 : Provoque des brûlures.
Phrases S :
S23 : Ne pas respirer les gaz/fumées/vapeurs/aérosols [terme(s) approprié(s) à indiquer par le fabricant].
S26 : En cas de contact avec les yeux, laver immédiatement et abondamment avec de l’eau et consulter un spécialiste.
S45 : En cas d’accident ou de malaise, consulter immédiatement un médecin (si possible, lui montrer l’étiquette).
S36/37/39 : Porter un vêtement de protection approprié, des gants et un appareil de protection des yeux/du visage.
|
| Phrases R : 34, |
| Phrases S : 23, 26, 36/37/39, 45, |
|
Unités du SI & CNTP, sauf indication contraire.
|
On appelle poly(styrène sulfonate) de sodium ou polystyrène sulfonate de sodium, abrégé en PSS, un polymère substitué du polystyrène dans lequel un groupe sulfonate –SO3– est fixé sur chaque atome de carbone n° 4 du groupe phényle des unités styrène, une fraction desquels porte un ion sodium Na+. Il se présente sous l'aspect d'un solide ou d'une poudre blanche, très soluble dans l'eau.
On l'obtient par polymérisation ou copolymérisation de styrène sulfonate, ou par sulfonation de polystyrène déjà polymérisé. Dans ce dernier cas, les conditions particulières sous lesquelles se déroule la sulfonation du polystyrène (par substitution électrophile aromatique en milieu acide chauffé) conduisent à la concurrence de multiples réactions parallèles, aboutissant à des substitutions doubles sur les noyaux phényles, même à des taux de sulfonation très inférieurs à 100 %, ainsi qu'à des réticulations entre groupes sulfonyle –SO2– condensés.
Le PSS est utilisé comme superplastifiant pour ciments et bétons, comme fixateur de teinture sur le coton, et comme membrane d'échange de protons dans les piles à combustibles.
Il peut également être utilisé pour accroître la solubilité de macromolécules apolaires dans certains procédés industriels requérant d'opérer en phase liquide, par exemple pour teindre une surface ou déposer une couche de polymère sur un matériau : on l'utilise ainsi avec le PEDOT pour former du PEDOT:PSS et réaliser certaines cellules photovoltaïques en polymères.
Notes et références
Articles liés
Wikimedia Foundation.
2010.
Contenu soumis à la licence CC-BY-SA. Source : Article Poly(styrène sulfonate) de sodium de Wikipédia en français (auteurs)
Regardez d'autres dictionnaires:
Poly(styrène sulfonate de sodium) — Poly(styrène sulfonate) de sodium Poly(styrène sulfonate) de sodium Unité de poly(styrène sulfonate) (l ion sodium Na+ n est pas représenté) Général … Wikipédia en Français
Poly(styrène sulfonate) — de sodium Poly(styrène sulfonate) de sodium Unité de poly(styrène sulfonate) (l ion sodium Na+ n est pas représenté) Général … Wikipédia en Français
Polystyrène sulfonate de sodium — Poly(styrène sulfonate) de sodium Poly(styrène sulfonate) de sodium Unité de poly(styrène sulfonate) (l ion sodium Na+ n est pas représenté) Général … Wikipédia en Français
Poly(3,4-ethylenedioxythiophene) — Poly(3,4 éthylènedioxythiophène) Poly(3,4 éthylènedioxythiophène) Deux maillons de PEDOT. Général No CAS … Wikipédia en Français
Poly(3,4-éthylènedioxythiophène) — Deux maillons de PEDOT. Général No CAS … Wikipédia en Français
Sodium polystyrene sulfonate — Systematic (IUPAC) name Poly(4 vinylbenzenesulfonate metal salt) Clinical data AHFS/ … Wikipedia
Poly(allylamine hydrochloride) — is a cationic polyelectrolyte that can be used in combination with an anionic polyelectrolyte like poly(sodium styrene sulfonate) to form a layer by layer adsorbed film of negatively and positively charged polymers … Wikipedia
28210-41-5 — Poly(styrène sulfonate) de sodium Poly(styrène sulfonate) de sodium Unité de poly(styrène sulfonate) (l ion sodium Na+ n est pas représenté) Général … Wikipédia en Français
PSS (polymère) — Poly(styrène sulfonate) de sodium Poly(styrène sulfonate) de sodium Unité de poly(styrène sulfonate) (l ion sodium Na+ n est pas représenté) Général … Wikipédia en Français
Polystyrènesulfonate — Poly(styrène sulfonate) de sodium Poly(styrène sulfonate) de sodium Unité de poly(styrène sulfonate) (l ion sodium Na+ n est pas représenté) Général … Wikipédia en Français


