- Particule elementaire
-
Proton
 Pour les articles homonymes, voir Proton (homonymie).
Pour les articles homonymes, voir Proton (homonymie).Proton 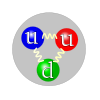
Propriétés générales Classification Particule composite (baryon) Composition 2 quarks u
1 quark dFamille Fermion Groupe Quark Interaction(s) Forte, électromagnétique, faible, gravitation Symbole p, p+ Antiparticule Antiproton Propriétés physiques Masse 938,272 MeV.c-2
(1,672 623×10-27 kg)Charge électrique 1,602 176 53×10-19 C Rayon de charge 0,875(7) fm Moment dipôlaire <5,4×10−24 e Cm Polarisabilité électrique 1,2(6)×10−3 fm³ Moment magnétique 2,792847351(28) μN Polarisabilité magnétique 1,9(5)×10−4 fm³ Charge de couleur 0 Spin ½ Isospin ½ Parité +1 Durée de vie Stable (supérieure à 1030 ans, voire à 1033ans) Historique Prédiction William Prout, 1815 Découverte 1918 Découvreur Ernest Rutherford Le proton est une particule subatomique portant une charge électrique élémentaire positive de 1,602×10-19 coulombs. Il fut découvert en 1919 par Ernest Rutherford.
Le noyau de l'isotope le plus répandu de l'atome d'hydrogène est un proton. Les noyaux des autres atomes sont composés de neutrons et de protons maintenus ensemble par la force forte.
Sommaire
Caractéristiques physiques
 Ernest Rutherford, le découvreur du proton.
Ernest Rutherford, le découvreur du proton.
Un proton a une masse de 1,672 623 1×10-27 kg, ce qui est environ 1 836,15 fois plus lourd qu'un électron. Son rayon serait de l'ordre de 0,8 femtomètre[1], pour des mesures plus précises les résultats divergent selon les méthodes employées.
Les protons sont classifiés comme des baryons et sont composés de deux quarks up et d'un quark down, qui sont maintenus ensemble par la force forte, transportée par les gluons. Sa charge électrique est de : 2/3e + 2/3e - 1/3e = 3/3e soit +e.
La force électromagnétique étant de nombreux ordres de grandeur plus forte que la gravitation, la charge d'un proton doit être égale à la charge d'un électron, sinon la répulsion nette provenant de l'excès de charge électrique positive ou négative aurait un effet notable sur l'expansion de l'univers et ainsi sur la matière agrégée gravitationnellement (planètes, étoiles, etc.). Il est acquis que le positron a la même charge que l'électron mais de signe opposé ; la même chose s'applique pour l'antiproton et le proton.
Lorsqu'un proton peut se désintégrer au sein d'un noyau par interaction faible, en vertu d'un bilan global d'énergie favorable, il donne trois particules : un positron, un neutron et un neutrino électronique (radioactivité β). C'est impossible pour un proton isolé, car le neutron est déjà plus lourd que le proton.
Sphéricité du proton
Jusqu'en 2003, les physiciens pensaient que le proton avait une forme sphérique. Or Gerald A. Miller a démontré que les protons n'étaient pas uniquement représentables par des petites boules chargées mais qu'ils pouvaient prendre d'autres formes comme celle d'un ballon de rugby[2].
Chimie
En chimie et en biochimie, le terme proton peut se référer à l'ion hydrogène en solution aqueuse (c'est-à-dire, l'ion hydronium). Dans ce contexte, un donneur de proton est un acide et un accepteur de proton est une base (voir les réactions acido-basiques). En effet, l'atome d'hydrogène dans son isotope ultra-majoritaire se compose d'un noyau formé d'un unique proton et sans neutron, et d'un cortège électronique d'un seul électron. Un atome d'hydrogène ayant perdu un électron est donc un proton libre. Dans une solution aqueuse, on ne peut pas vraiment distinguer l'ion hydronium H3O+ et le proton H+, ce dernier ayant tendance à former constamment des liaisons avec les molécules d'eau (et les molécules d'eau étant ultra-majoritaires, il est inutile de tenir compte de la formation des ions H3O+ pour calculer le nombre de molécules d'eau).
Un acide 'monoprotique' (chlorure d'hydrogène, acide éthanoïque, acide nitrique) ne peut céder qu'un seul proton par molécule.
Notes et références de l'article
Voir aussi
Articles connexes
Liens et documents externes
- (fr) Analyse de la mesure du rayon d'un proton sur le site du CNRS
- [pdf] (en) Caractéristiques du proton (Particle Data Group)
- Portail de la chimie
- Portail de la physique
Catégories : Acide | Cation | Chimie des solutions | Chimie nucléaire | Hadron | Physique nucléaire | Radioactivité
Wikimedia Foundation. 2010.
