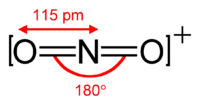
- Ion nitronium
-
L’ion nitronium NO2+ est un oxycation azoté instable dans les conditions normales. Il résulte de l'arrachement d'un électron à une molécule de dioxyde d'azote NO2 ou de la protonation de l'acide nitrique HNO3.
Il intervient dans la réaction de nitration, notamment dans celle des composés aromatiques. On peut le mettre en évidence par spectroscopie dans les mélanges d'acide sulfonitrique selon la réaction suivante :
 Mécanisme de formation de l'ion nitronium.
Mécanisme de formation de l'ion nitronium.
L'ion nitronium existe aussi sous la forme solide de pentoxyde d'azote N2O5, qui est un solide ionique formé d'ions nitronium et nitrate. Ses formes liquide et gazeuse, cependant, sont moléculaires et ne contiennent pas d'ion nitronium. Quelques sels de nitronium formés avec des anions faiblement nucléophiles, comme le perchlorate de nitronium, [NO2+][ClO4-] peuvent être isolé mais sont extrêmement réactifs.
L'ion nitronium est isoélectronique avec le dioxyde de carbone et, comme ce composé, a un structure linéaire : l'enchainement O=N=O forme un angle de 180° (voir la théorie VSEPR).
Les composés NO2F (fluorure de nitrile) et NO2Cl (chlorure de nitrile) ne sont pas des sels de nitronium mais plutôt des composés moléculaires, comme le montrent leurs bas points d'ébullition (respectivement, de -72 °C et de -6 °C) et la faible longueur des liaisons N-X (N-F 135 pm, N-Cl 184 pm)[1].
L'addition d'un électron forme le radical neutre NO2· ; en fait, celui-ci est assez stable et est connu sous le nom de dioxyde d'azote.
L'espèce négativement chargée est NO2-, l'ion nitrite.
Notes et références
- F.A.Cotton and G.Wilkinson, Advanced Inorganic Chemistry, 5th edition (1988), Wiley, p.333
Catégories :- Oxycation
- Composé de l'azote
Wikimedia Foundation. 2010.