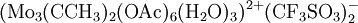- Couplage oxydatif
-
Réaction de couplage
Une réaction de couplage ou couplage oxydatif en chimie organique est un nom générique pour une catégorie de réactions en chimie organométallique dans laquelle deux radicaux hydrocarbures sont couplés avec l'aide d'un catalyseur contenant un métal.
Les réactions de couplage doivent être divisés en deux types principaux : les couplages croisés et les homocouplages.Les couplages croisés concernent deux molécules différentes réagissant pour former une nouvelle molécule. On peut citer par exemple une réaction catalysée par chlorure de nickel d'un halogénure d'aryl-magnésium avec un halogénure d'aryle pour former un diaryle.
La réaction d'Ullmann est d'un exemple d'homocouplage : il s'agit de la réaction catalysée par du cuivre métallique de deux molécules d'un halogénure d'aryle afin de former un biaryle. La réaction d'Ullmann nécessite parfois de très hautes températures, et peut être parfois remplacée en chimie de synthèse par des réactions catalysée par du palladium.De nombreuses réactions de couplage concernent les phénols. Le BINOL est le produit de réaction C-C du 2-naphthol avec du chlorure de cuivre (II) et le 2,6-xylénol dimérise avec le diacétate d'iodosobenzène.
Un des métaux communs dans ce type de chimie est le palladium, parfois ajouté sous la forme du tétrakis(triphénylphosphine) palladium (0). C'est un composé sensible à l'air particulièrement performant dans le couplage de composés halogénés non-saturés comme l'hydrure de tributyle-étain.
Alors que de nombreuses réactions de couplage impliquent des réactifs extrêmement sensibles à la présence d'eau ou d'oxygène, il est raisonnable d'affirmer que toutes les réactions de couplages doivent être réalisées en stricte absence d'eau. Il est possible de réaliser des réactions de couplage avec du palladium dans des solutions aqueuses en utilisant des phosphines sulfonées solubles dans l'eau synthétisées par la réaction de la triphénylphosphine avec de l'acide sulfurique. En général, l'oxygène de l'air est encore plus capable de faire avorter les réactions de couplages : en effet, nombre de ces réactions se produisent grâce à des complexes de métaux insaturés ne possédant pas 18 électrons de valence. Ainsi, les couplages croisés par nickel ou palladium un complexe à valence nulle avec deux sites vacants (ou ligands labiles) réagit avec la liaison carbone-halogène afin de former une liaison métal-halogène et une liaison métal-carbone. Un tel complexe à valence zéro avec des ligands labiles ou des sites de coordination vides est normalement très réactif à l'oxygène.
Types de couplages
Les réactions de couplages incluent (liste non exhaustive):
Réaction année Réactif A Réactif B homo-/croisé catalyseur remarque Réaction de Wurtz 1855 R-X sp3 homo- Na Couplage de Glaser 1869 R-X sp homo- Cu Réaction d'Ullmann 1901 R-X sp2 homo- Cu Réaction de Gomberg-Bachmann 1924 R-N2X sp2 homo- Base requise Couplage de Cadiot-Chodkiewicz 1957 alcyne sp R-X sp croisé Cu Base requise Couplage de Castro-Stephens 1963 R-Cu sp R-X sp2 croisé Couplage de Kumada 1972 R-MgBr sp2, sp3 R-X sp2 croisé Pd ou Ni Réaction de Heck 1972 alcène sp2 R-X sp2 croisé Pd Base requise Couplage de Sonogashira 1973 alcyne sp R-X sp3 sp2 croisé Pd et Cu Base requise Couplage de Negishi 1977 R-Zn-X sp2 R-X sp3 sp2 croisé Pd ou Ni Couplage croisé de Stille 1977 R-SnR3 sp2 R-X sp3 sp2 croisé Pd Base requise Réaction de Suzuki 1979 R-B(OR)2 sp2 R-X sp3 sp2 croisé Pd Base requise Couplage de Hiyama 1988 R-SiR3 sp2 R-X sp3 sp2 croisé Pd Base requise Réaction de Buchwald-Hartwig 1994 R2N-SnR3 sp R-X sp2 croisé Pd Couplage N-C, la seconde génération libère l'amine. Aperçu des réactions de couplages. Voir les liens pour les références Réactions diverses
Dans une étude, une réaction de couplage inhabituelle a été décrite[1] dans laquelle un composé organomolybdénien :
est non seulement resté sur une étagère pendant 30 ans sans aucun signe de dégradation mais s'est aussi décomposé dans l'eau pour générer du 2-butyne qui est l'adduit de couplage de ses deux ligands éthylidyne. Cela ouvre, selon les chercheurs, une autre voie pour la chimie organométallique aqueuse.
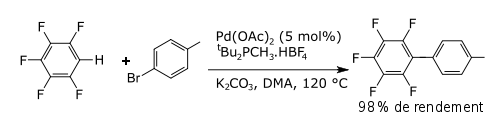
Une méthode pour les réactions de couplages croisés des halogénures d'aryles avec des arènes fluorés catalysées par palladium utilisent du DMA. Elle est inhabituelle du fait qu'elle comprend une fonctionnalisation sur une arène déficitaire en électrons[2].
Références et notes
- ↑ Formation of a Carbon-Carbon Triple Bond by Coupling Reactions In Aqueous Solution Avi Bino, Michael Ardon, Elijah Shirman Science, 2005, V308(5719), 234-235
- ↑ Catalytic Intermolecular Direct Arylation of Perfluorobenzenes Marc Lafrance, Christopher N. Rowley, Tom K. Woo, and Keith Fagnou J. Am. Chem. Soc.; 2006; 128(27) pp 8754 - 8756; (Communication) DOI:10.1021/ja062509l
- (en) Cet article est partiellement ou en totalité issu d’une traduction de l’article de Wikipédia en anglais intitulé « Coupling reaction ».
- Portail de la chimie
Catégories : Réaction formant une liaison carbone-carbone | Réaction formant une liaison carbone-hétéroatome | Chimie organométallique | Catalyse
Wikimedia Foundation. 2010.