- Chlorure de soufre(I)
-
Chlorure de soufre
Chlorure de soufre 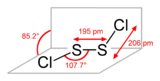
Général Nom IUPAC dichlorure de disoufre No CAS No EINECS Apparence liquide fumant, huileux, ambre a rouge, d'odeur acre.[1] Propriétés chimiques Formule brute S2Cl2 Masse molaire 135,036 g∙mol-1
Cl 52,51 %, S 47,49 %,Propriétés physiques T° fusion -77 °C[1] T° ébullition 138 °C[1] Solubilité dans l'eau : réaction[1] Masse volumique (eau = 1) : 1.7[1] T° d’auto-inflammation 234 °C[1] Point d’éclair 118 °C c.f.[1] Pression de vapeur saturante à 20 °C : 0.90 kPa[1] Précautions Directive 67/548/EEC 
T
C
NPhrases R : 14, 20, 25, 29, 35, 50, Phrases S : (1/2), 26, 36/37/39, 45, 61, Transport - 1828 NFPA 704 SIMDUT[2] 

SGH[3] 


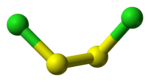
DangerUnités du SI & CNTP, sauf indication contraire. Le dichlorure de disoufre a pour formule S2Cl2. on l'appelle aussi (mono)chlorure de soufre , Nom impliqué par sa formule empirique SCl. S2Cl2 a une structure pliée dans laquelle l'angle entre les plan Cla-S-S et S-S-Clb est de environ 90 °. On dit que cette structure est gauche et elle est comparable à celle de H2O2. L'isomère de S2Cl2, S=SCl2, apparaît brièvement lors de l'exposition de S2Cl2 aux UV.
Sommaire
Synthèse
S2Cl2 se forme par chloration ménagée du soufre:
-
- S8 + 4 Cl2 → 4 S2Cl2 ΔH = -58.2 kJ/mol
- S2Cl2 + Cl2 → 2 SCl2 ΔH = -40.6 kJ/mol
Comme indiqué ci dessus, un excès de Cl2 convertit S2Cl2 en SCl2. Ces deux réactions sont réversibles. S2Cl2 est un sous produit de la chloration du disulfure de carbone dans la synthèse du thiophosgéne.
Propriétés
Le dichlorure de soufre est incolore à l'état pur mais les échantillons impurs sont souvent jaunes. Il se décompose en émettant de la fumée dans l'air humide à cause d'une réaction avec l'eau:
-
- 2 S2Cl2 + 2 H2O → SO2 + 4 HCl + 3/8 S8
Applications en synthèse
S2Cl2 a été utilisé pour introduire des liaisons C-S. En présence de chlorure d'aluminium, S2Cl2 réagit avec le benzène pour donner le disulfure de diphényle :
-
- S2Cl2 + C6H6 → (C6H5)2S + 2 HCl + 1/8 S8
Les Anilines réagissent avec S2Cl2 en présence de NaOH pour donner des ortho-aminothiophenolates suivant la réaction de herz, précurseur des colorants thioindigotiques. On s'en sert aussi pour préparer le gaz moutarde en le faisant réagir avec l'éthylène:
-
- S2Cl2 + 2 C2H4 → (ClC2H4)2S + 1/8 S8
Utilisation
Le chlorure de soufre entre dans la composition d'additifs destinés à des lubrifiants soumis à de fortes pressions. Il est aussi employé pour vulcaniser le caoutchouc. On le retrouve également dans les insecticides ainsi que l'industrie pharmaceutique.
Références
- (en)Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- (en)W. W. Hartman, L. A. Smith, and J. B. Dickey "Diphenylsulfide" Organic Syntheses, Coll. Vol. 2, p. 242; Vol. 14, p. 36.
- (en)R. J. Cremlyn “An Introduction to Organosulfur Chemistry” John Wiley and Sons: Chichester (1996). ISBN 0-471-95512-4
- (en)Garcia-Valverde M., Torroba T., « Heterocyclic chemistry of sulfur chlorides - Fast ways to complex heterocycles », dans European J. Org. Chem., vol. 4, 2006, p. 849-861
- ↑ a , b , c , d , e , f , g et h MONOCHLORURE DE SOUFRE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Chlorure de soufre » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Portail de la chimie
Catégories : Produit chimique toxique | Produit chimique corrosif | Produit chimique dangereux pour l'environnement | Composé du soufre | Chlorure -
Wikimedia Foundation. 2010.