- 95-13-6
-
Indène
Indène 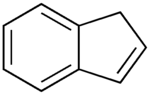
Général Synonymes Benzocylopentadiène
IndonaphtèneNo CAS No EINECS PubChem Propriétés chimiques Formule brute C9H8 Masse molaire 116,1598 g∙mol-1
C 93,06 %, H 6,94 %,Propriétés physiques T° fusion -1,7 °C[1] T° ébullition 182,6 °C[1] Solubilité quasi-insoluble dans l'eau Masse volumique 0,996 g∙cm-3 à 20 °C[1] Point d’éclair 58,00 °C (coupelle fermée)[1] Pression de vapeur saturante 2 mbar à 20 °C
2,9 mbar à 30 °C
9 mbar à 50 °C [2]Précautions Directive 67/548/EEC 
XnPhrases R : 10, 65, Transport 33/30 3295 Unités du SI & CNTP, sauf indication contraire. L'indène est un hydrocarbure bicyclique de formule C8H9. Il se présente sous la forme d'un liquide incolore à jaune pâle. Il est composé d'un cycle benzénique fusionné avec une cycle de cyclopentadiène.
Son nom provient de la contraction de indonaphthène.
Sommaire
Synthèse/extraction
L'indène est naturellement présent dans les fraction du goudron bouillant entre 175 °C et 185 °C. Il peut être obtenu en chauffant cette fraction avec du sodium, qui précipite sous forme de « sodio-indène ». Cette réaction utilise les propriétés d'acide faible de l'indène, par sa déprotonation par le sodium. Le sodio-indène est ensuite reconvertit en indène par distillation à la vapeur.[3]
Réactivité
L'indène, en particulier le 2H-indène se dimérise rapidement à l'air libre ou à la lumière. L'oxydation de l'indène par le dichromate acide donne l'acide homophthalique. Il se condense avec l'oxalate d'éthyle en présence d'éthoxyde de sodium pour former un ester indene-oxalique. Il se condense également avec des composés carbonylés (cétones, aldéhydes) en miliue alcalin pour former des benzofulvènes (composés extrêmement colorés). L'indène peut aussi être transformé en anion indène qui est utilisé chimie organométallique, où il est considéré comme un bon ligand, dû à l'effet indényle.
Utilisations
L'indène est utilisé comme solvant pour des réactions organiques. Il est utilisé pour la synthèse de résines indène-coumarone. Il sert de ligand pour les métaux de transition en catalyse homogène. C'est aussi un réactif pour la synthèse de l'azulène.
Notes et références
- ↑ a , b , c et d [1]
- ↑ Entrée de « Indene » dans la base de données de produits chimiques GESTIS de la BGIA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 12/05/2009 (JavaScript nécessaire)
- ↑ (en) Gerd Collin, Rolf Mildenberg, Mechthild Zander, Hartmut Höke, William McKillip, Werner Freitag, Wolfgang Imöhl “Resins, Synthetic” Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim, 2000.
- (de) Cet article est partiellement ou en totalité issu d’une traduction de l’article de Wikipédia en allemand intitulé « Inden (Verbindung) ».
- (en) Cet article est partiellement ou en totalité issu d’une traduction de l’article de Wikipédia en anglais intitulé « Indene ».
Voir aussi
- Indane
- Indole
- Isoindène
- Effet indényle
- Portail de la chimie
Catégories : Produit chimique nocif | Hydrocarbure
Wikimedia Foundation. 2010.

