- C47H72O14
-
Ivermectine
Ivermectine 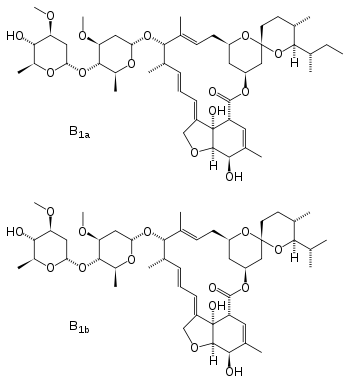
Général Nom IUPAC Ivermectine (22,23-dihydroavermectin B1a + 22,23-dihydroavermectin B1b) No CAS No EINECS Code ATC DrugBank PubChem SMILES InChI Apparence Solide Propriétés chimiques Formule brute C48H74O14 (22,23-dihydroavermectin B=1a)
+ C47H72O14 (22,23-dihydroavermectin B=1b)Masse molaire 875.10 g/mol Propriétés physiques T° fusion 155 °C Solubilité Insol dans l'eau Précautions Directive 67/548/EEC 
TPhrases R : 25, 36, 61, Phrases S : 26, 45, 53, Écotoxicologie DL50 25 mg/kg souris oral
30 mg/kg souris i.p.Données pharmacocinétiques Liaison protéique 93% Considérations thérapeutiques Voie d’administration Orale Unités du SI & CNTP, sauf indication contraire. L'Ivermectine est un médicament utilisé pour traiter des parasitoses mais aussi la gale.
L'Ivermectine est un antihelminthique dérivé des avermectines isolées à partir de la fermentation de Streptomyces avermitilis.[1] Sa formule chimique brute est C95H146O28 [2]
En France, l'Ivermectine est commercialisé par le laboratoire MSD sous les dénominations commerciales Mectizan © [3] et Stromectol © [4]
Sommaire
Pharmacodynamie
L’ Ivermectine est une molécule apparentée aux avermectines (Insecticides souvent utilisés à usage domestique comme appâts contre les fourmis ) qui sont extraites d’une bactérie le Streptomyces avermitilis. L’Ivermectine a un effet toxique par son action sur le système nerveux et la fonction musculaire, elle agit en particulier en inhibant la neurotransmission. La molécule présente une affinité importante pour les canaux chlorures glutamate-dépendants présents dans les cellules nerveuses et musculaires des invertébrés(Cully et coll, 1994 ; Cully et coll, 1997, Dent et coll, 1997), avec pour conséquence la paralysie et la mort par atteinte neuro-musculaire. Les mutations qui réduisent l’action de l'ivermectine sur les canaux chlorures confèrent une résistance à cette molécule(Dent et coll, 2000, Kane et coll, 2000). Bien qu’ayant une structure semblable à celle des récepteurs à glycine des canaux ioniques des vertébrés, les canaux chlorures glutamate-dépendants sont spécifiques des invertébrés (bosselure, 2006). L'absence de canaux chlorures glutamate-dépendants chez les mammifères semble rendre compte en partie de la spécificité de l’action de l'ivermectine sur les parasites invertébrés et son manque relatif d'effets secondaires sur leurs hôtes mammifères (Lerchner et coll, 2007). L’ivermectine interagit également avec des canaux chlorures ligand-dépendants faisant intervenir le neuro-médiateur GABA (acide gamma-amino-butyrique)bien que leur importance soit encore peu claire (Ludmerer et autres., 2002, Blackhall 2003). Le récepteur périphérique principal des neurotransmetteurs chez les mammifères, le récepteur nicotinique de l'acétylcholine, est relativement peu affecté par la molécule (MSD, 1988), ce qui contribue à son innocuité pour l'homme.
Pharmacocinétique
L’Ivermectine peut être administrée soit par voie orale ou par voie parentérale. Elle ne franchit pas facilement la barrière hématoméningée chez les mammifères (Schinkle et coll, 1994), bien que le passage puisse devenir significatif si l'ivermectine est prescrite à des doses élevées (dans ce cas, le pic au niveau du cerveau est atteint 2 à 5 heures après l’administration).
Toxicité
Le risque principal est celui de la neurotoxicité, qui chez la plupart des espèces de mammifères peut se manifester par une dépression du systême nerveux central (SNC), avec pour conséquence une ataxie, comme on aurait pu s'y attendre du fait de la potentialisation des synapses inhibitrices du système GABA-ergique (Hayes et Laws, 1991). En général on utilise les pesticides sous forme de spécialités contenant plusieurs substances;ces préparations sont classées par l’Agence de protection de l'environnement des États-Unis comme toxiques de catégorie IV, c’est-à-dire très faiblement toxiques. Ceci signifie que bien que fortement toxiques pour les insectes, les préparations de pesticides contenant de l'ivermectine ne devraient généralement pas avoir d’ effet nuisible pour les mammifères en mode normal d’utilisation. Par exemple, on peut déterminer pour une telle préparation une DL50 (dose létale 50) par voie orale de 650 mg/kg chez le rat( toxicité classée en catégorie III : basse toxicité) [1]. Extrapolé à l’homme pour un poids de 80 kilogrammes, la dose létale 50 est de 52 g, soit approximativement le poids et le volume de l'iPod nano, ce qui est considéré par l'EPA comme correspondant à une faible toxicité. Cependant, les préparation d'avermectine pure (par opposition aux formulations de pesticides dilués) sont fortement toxiques à la fois pour les insectes et pour les mammifères (également pour la vie aquatique, et les poissons). Une étude indique une LD50 par voie orale de 10 mg/kg chez les rats (ce qui correspond à la catégorie I de toxicité ; toxicité élevée) [2]. Certaines races de chiens plus particulièrement le colley, présentent des signes d'atteinte toxique du système nerveux central après exposition à des doses d'ivermectine dépassant 150 à 200 µg /kg. [3] La cause de cette toxicité pour le SNC chez les chiens sensibles au produit a été attribuée à une mutation d’un gène responsable de la synthèse d’une protéine de multi résistance aux médicaments. [4] Ceci a conduit certains à conclure que les colleys ne devraient pas être traités avec l'ivermectine ou aucune autre avermectine. Les spécialités vétérinaires d'ivermectine généralement prescrites et utilisées pour la prophylaxie de la filaire du chien(Dirofilaria repens)sont dosés de 6 à 12 µg/kg [5] et sont généralement considérées comme inoffensives. Un surdosage grave d'ivermectine est nécessaire pour que se produisent les effets toxiques de l'ivermectine. [6] Un test est disponible pour vérifier la sensibilité des chiens à l'ivermectine ainsi qu’à plusieurs autres médicaments. [7] (voir P-glycoprotéine)
Toxicité pour l'environnement
L'ivermectine est extrêmement toxique pour les insectes et les organismes aquatiques.
Administrée aux bovins, ovins et chevaux, elle est majoritairement éliminée par voie fécale, et les concentrations dans les bouses et crottins sont élevées pendant les jours qui suivent le traitement. La durée d'élimination dans les excréments des animaux traités dépend de la voie d'administration du médicament(intra-musculaire, pour-on, bolus) et varie entre 10 et 150 jours. L'impact très négatif de l'ivermectine sur la faune non-cible (diptères et coléoptères copropophages (=bousiers)) a été établi par de très nombreuses études, même si le laboratoire qui la commercialise a publié quelques études contradictoires.
En raison de cette écotoxicité, le bolus pour bovins, la forme qui engendrait la persistance la plus longue dans les bouses, a été retiré du marché, en France, en 2003. Demeurent en 2009 sur le marché français les formes suivantes : pâte orale pour chevaux, solution pour-on, solution injectable
Pour limiter les impacts de l'ivermectine sur la faune non-cible, certains auteurs conseillent de garder les animaux enfermés pendant les jours qui suivent le traitement, ou de remplacer le traitement à l'ivermectine par des traitements anti-parasitaires moins toxiques (moxidectine, benzimidazolés), voire de limiter le nombre de traitement annuel grâce à des techniques d'élevage (et de lutte antiparasitaire) adaptées, reposant sur la rotation des pâtures.[5]
Indications thérapeutiques
En médecine humaine
L’Ivermectine est un antiparasitaire à large spectre. Il est principalement utilisé chez l'homme pour le traitement des maladies suivantes :
- l’onchocercose à Onchocerca volvulus
- La Filariose lymphatique à Wuchereria bancrofti
- anguillulose ou strongyloïdose
- l’ascaridiose
- la trichocéphalose et l’oxyurose
- Larva migrans cutanée
- La gale est une dermatose prurigineuse dont le traitement repose sur des topiques locaux. L'ivermectine s'est avérée efficace pour le traitement oral de cette affection.[6]
Les données en faveur de cette utilisation non conforme aux préconisations initiales sont plus récentes. La molécule est active sur les acariens comme le sarcoptes de la gale. Au départ cette indication était limitée aux cas qui s’avèraient résistants aux traitements locaux et/ou qui se présentaient sous une forme étendue (comme la gale norvégienne). Sa facilité d’utilisation (dose orale unique) a permis d’étendre ces indications vers le traitement des formes communes.
Posologie
- Adultes
- Par voie orale: 3 à 12 mg en dose unique (environ 150 à 200µg/kg de masse corporelle) pour l’onchocercose et les autres infections parasitaires. (par exemple 6,75 à 9 mg pour un adulte de 45 kg)
- Enfants
- L’Ivermectine n’est pas prescrite aux enfants de moins de 15 kg. Pour les enfants plus grands, la dose est de 150 µg/ kg de masse corporelle.
- Contrindications
- L’Ivermectine est contrindiquée chez les personnes qui présentent une hypersensibilité immédiate au médicament. Elle ne doit pas être prescrite à des mères qui allaitent un nourrissson de moins de trois mois (Reynolds, 1993).
En médecine vétérinaire
Chiens
L’Ivermectine est la principale substance utilisée pour la prévention de la filaire du chien, une dose est donnée chaque mois à l’animal pour empêcher le développement du parasite à l'étape tissulaire des microfilaires. Certaines races de type-Colley sont apparemment plus sensibles à l'ivermectine, et les vétérinaires prescrivent pour eux d'autres types de traitements préventifs de la filaire. Ceci concerne le border collie, le berger shetland et beaucoup d’autres races de chiens de berger.
Chevaux
L’Ivermectine est une substance très répandue dans certains vermifuges pour les chevaux, avec des noms de marques commerciales comme Equimax, Equimectrin, Eqvalan, et Zimecterin. Il est généralement administré par voie orale sous forme d’une pâte déposée directement dans la bouche de l'animal par l'intermédiaire d'une seringue. L'Ivermectine protège contre la plupart des parasites internes du cheval, y compris leur larves, excepté les vers plats.
Rongeurs
Le traitement le plus utilisé contre l’infestation des fourrures des rongeurs par les acariens est actuellement basé sur l'administration orale ou parentérale d’avermectines, une famille de lactones macrocycliques produites par la fermentation d’un micro-organisme tellurique le streptomyces avermitilis. Ils ont une activité contre une large gamme de nématodes et d'arthropodes parasites des animaux domestiques à la concentration de 300 µg/kg ou moins. À la différence des antibiotiques du groupe des macrolides ou des polyènes (antifongiques), ils n’ont pas d'activité antibactérienne ou antifongique significative(Hotson, 1982). L’usage thérapeutique des Avermectines n'est pas sans inconvénient. La résistance aux avermectins a été rapportée, ce qui suggère d’en modérer l'utilisation (Clark, 1995). La recherche sur l'ivermectine, la pipérazine, et le dichlorvos utilisés en association montre également une toxicité potentielle(Toth, 2000). On a rapporté que les Avermectines bloquent la sécrétion LPS-induite du facteur TNF (facteur onconécrosant), du NO (monoxyde d’azote), de la prostaglandine E2, et augmente la concentration intracellulaire de Ca2+ (Victorov, 2003). Une méthode efficace de réduction des ectoparasites qui soumettrait les animaux de laboratoire à moins de contraintes que l'administration par voie orale d'avermectine est certainement souhaitable.
Oiseaux
L’Ivermectine est généralement utilisée pour traiter les infestations par acariens chez les oiseaux, habituellement pour des dermatoses squameuses de la face ou des pattes dues à un parasite le Cnemidocoptes. Dans de nombreux pays cette indication constitue une utilisation non conforme aux recommandations.
Sources
- ↑ RCP du produit
- ↑ Molécule du Stromectol ©
- ↑ Note du dictionnaire Vidal © sur Mectizan ©
- ↑ Note du dictionnaire Vidal © sur Stromectol ©
- ↑ Virlouvet G. 2005. Le Point Vétérinaire. 255. 42-45
- ↑ Résumé de l'étude mexicaine de Macotela-Ruiz
References
- Mectizan Donation Program
- Ivermectin data sheet (source of structural formula)
- Ivermectin for human use
- Site profiling ivermectin and avermectin as pesticides
- Toxicity information for avermectin
- Medline Plus Information
- U.S. National Library of Medicine. Hazardous Substances Databank. Bethesda, MD, 1995.10-9
- Lankas, G. R and Gordon, L. R. Toxicology. In Ivermectin and Abamectin. Campbell, W. C., Éd. Springer Verlag, New York, NY, 1989.10-142
- U.S. Environmental Protection Agency. Pesticide Fact Sheet Number 89.2: Avermectin B1. Office of Pesticides and Toxic Substances, Washington, DC, 1990.10-143
- U.S. Environmental Protection Agency. Pesticide Fact Sheet Number 89.2: Avermectin B1. Office of Pesticides and Toxic Substances, Washington, DC, 1990.10-143
- Clark JM, 1995, with Scott JG, Campos F, Bloomquist JR, Resistance to avermectins: extent, mechanisms, and management implications, Annu Rev Entomol, 40:1-30.
- Toth LA, 2000, with Oberbeck C, Straign CM, Frazier S, Rehg JE, Toxicity evaluation of prophylactic treatments for mites and pinworms in mice, Contemp Top Lab Anim Sci., Mar;39(2):18-21.
- Viktorov AV, 2003, with Yurkiv VA, Effect of ivermectin on function of liver macrophages, Bull Exp Biol Med., Dec;136(6):569-71.
- Viktorov AV, 2003, with Yurkiv VA, Effect of ivermectin on function of liver macrophages, Bull Exp Biol Med., Dec;136(6):569-71.
- Cully, D.F., Vassilatis, D.K., Liu, K.K., Paress, P.S., Van der Ploeg, L.H., Schaeffer, J.M., Arena, J.P., 1994. Cloning of an avermectin-sensitive glutamate-gated chloride channel from Caenorhabditis elegans. Nature. 371(6499):707-11.
- Cully, D.F., Paress, P.S., Liu, K.K., Schaeffer, J.M., Arena, J.P., 1996. Identification of a Drosophila melanogaster glutamate-gated chloride channel sensitive to the antiparasitic agent avermectin. J.f Biol. Chem. 271(33):20 187-91.
- Dent, J.A., Davis, M. Wayne & Avery, L.A., 1997. avril-15 encodes a chloride channel subunit that mediates inhibitory glutamatergic neurotransmission and ivermectin sensitivity in Caenorhabditis elegans. EMBO J. 16(19): 5867-5879.
- Dent, J.A., Smith, M., Vassilatis, D.K. and Avery, L., 2000. The genetics of ivermectin resistance in Caenorhabditis elegans. Proc. Nat. Acad. Sci. USA 97(6): 2674-2679.
- Dent, J.A., 2006. Evidence for a diverse cys-loop ligand-gated ion channel superfamily in early bilateria. J. Mol. Evol.62:523-535.
- Kane, N.S., Hirschberg, B., Qian, S., Hunt, D., Thomas, B., Brochu, R., Ludmerer, S.W., Zheng, Y., Smith, M., Arena, J.P., Cohen, C.J., Schmatz, D., Warmke, J., Cully, D.F., 2000. Drug-resistant Drosophila indicate glutamate-gated chloride channels are targets for the antiparasitics nodulisporic acid and ivermectin. Proc. Nat. Acad. Sci. USA 97(25):13 949-54.
- Lerchner, W., Xiao, C., Nashmi, R., Slimko, E.M., van Trigt, L., Lester, H.A., and Anderson, D.J., 2007. Reversible silencing of neuronal excitability in behaving mice by a genetically targeted, ivermectin-gated Cl− channel. Neuron, 54(1)1: 35-49.
- Ludmerer, S.W., Warren. V.A., Williams, B.S., Zheng, Y., Hunt, D.C., Ayer, M.B., Wallace, M.A., Chaudhary, A.G., Egan, M.A., Meinke, P.T., Dean, D.C., Garcia, M.L... Cully, D.F., Smith, M.M., 2002. Ivermectin and nodulisporic acid receptors in Drosophila melanogaster contain both gamma-aminobutyric acid-gated Rdl and glutamate-gated GluCl alpha chloride channel subunits. Biochemistry. 41(20):6548-60.
- Schinkel, A.H. Smit, J.J., van Tellingen, O., Beijnen, J.H., Wagenaar, E., van Deemter, L., Mol, C.A., van der Valk, M.A., Robanus-Maandag, E.C., Riele, H.P., et al., 1994. Disruption of the mouse mdr1a P-glycoprotein gene leads to a deficiency in the blood-brain barrier and to increased sensitivity to drugs. Cell. 77(4):491-502.
- Portail de la médecine
- Portail de la pharmacie
Catégories : Produit chimique toxique | Produit chimique reprotoxique | Antihelminthique
Wikimedia Foundation. 2010.
