- 31366-25-3
-
Tétrathiafulvalène
Tétrathiafulvalène 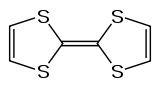
Structure du tétrathiafulvalène Général Nom IUPAC 2-(1,3-dithiol-2-ylidène)-1,3-dithiole Synonymes Δ2,2′-Bi-1,3-dithiole, TTF No CAS No EINECS PubChem SMILES InChI Apparence cristaux orange Propriétés chimiques Formule brute C6H4S4 [Isomères] Masse molaire 204,356 g∙mol-1
C 35,26 %, H 1,97 %, S 62,77 %,Propriétés physiques T° fusion 190,1 à 191,3 °C [1] Thermochimie ΔfH0solide 290,8 kJ∙mol-1 [2] PCI -5 619,5 kJ∙mol-1[2] Précautions NFPA 704 SIMDUT[3] Produit non contrôlé Unités du SI & CNTP, sauf indication contraire. Le tétrathiafulvalène, généralement abrégé en TTF, est un composé chimique hétérocyclique contenant du soufre de formule H2C2S2C=CS2C2H2. Il est étudié intensivement en électronique moléculaire comme donneur d'électrons (composé de type p), notamment dans le cadre des complexes à transfert de charge qu'il forme avec le TCNQ. Le TTF et ses dérivés forment notamment des sels de Bechgaard, qui deviennent supraconducteurs à basse température : c'est particulièrement le cas du TMTSF (tétraméthyltétrasélénafulvalène) et du BEDT-TTF (bis(éthylènedithio)-tétrathiafulvalène). Plus de dix milles publications scientifiques traitent du TTF et de ses dérivés[4].
Préparation
L'intérêt porté au TTF et à ses dérivés a conduit au développement de plusieurs synthèses de cette molécule et de ses analogues[4]. La plupart de ces préparations passent par le couplage de molécules ayant un noyau C3S2 cyclique comme les 1,3-dithiol-2-thiones ou les 1,3-dithiol-2-ones associées. Pour le TTF, la synthèse commence avec le trithiocarbonate H2C2S2C=S, qui est d'abord S-méthylé puis traité au tétrafluoroborate d'hydrogène HBF4 et enfin à la triéthylamine[5] :
- H2C2S2CH(SCH3) + HBF4 → [H2C2S2CH+]BF4- + HSCH3
- 2 [H2C2S2CH+]BF4- + 2 Et3N → H2C2S2C=CS2C2H2 + 2 Et3NHBF4
Notes et références
- ↑ (en) F. Wudl, M. L. Kaplan, E. J. Hufnagel et E. W. Southwick, Jr., « A Convenient Synthesis of 1,4,5,8-Tetrahydro- 1,4,5,8-tetrathiafulvalene », dans The Journal of Organic Chemistry, vol. 39, no 25, 1er août 1974, p. 3608-3609 [texte intégral (page consultée le 22 janvier 2009)]
- ↑ a et b Tetrathiafulvalene sur http://www.nist.gov/. Consulté le 22 janvier 2009
- ↑ « Tétrathiafulvalène » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ a et b M. Bendikov, F. Wudl, D. F. Perepichka, « Tetrathiafulvalenes, Oligoacenenes, and Their Buckminsterfullerene Derivatives: The Brick and Mortar of Organic Electronics », dans Chemical Reviews, vol. 104, 2004, p. 4891–4945 [lien DOI]
- ↑ Wudl, F.; Kaplan, M. L., « 2,2'Bi-1,3-dithiolylidene (Tetrathiafulvalene, TTF) and Its Radical Cation Derivatives », dans Inorg. Synth., vol. 19, 1979, p. 27–30 [lien DOI]
Articles liés
- Électronique moléculaire
- TCNQ – Tétracyanoquinodiméthane
- Portail de la chimie
- Portail de l’électricité et de l’électronique
Catégories : Composé hétérocyclique comportant du soufre | Semi-conducteur organique
Wikimedia Foundation. 2010.

