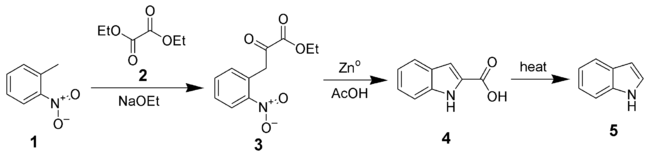
- Synthèse de Reissert de l'indole
-
La synthèse de Reissert de l'indole est une série de réactions chimiques permettant de substituer l'indole (5) ou d'un indole substitué (4) à partir de l'orthonitrotoluène (1) et de l'oxalate de diéthyle (2)[1],[2]. Proposée en 1897, la synthèse de Reissert est l'une des première à permettre la synthèse d'indole non substitué.
Il a été montré que l'utilisation d'éthanolate de potassium donne de meilleurs résultats que l'éthanolate de sodium[3].
Mécanisme réactionnel
Au cours de la première étape, le groupement méthyle de l'orthonitrotoluène (1) est déprotoné en milieu fortement basique (présence d'éthanolate sous la forme NaOEt), ce qui permet sa condensation avec le diéthyloxalate (2) pour former l'éthyl o-nitrophénylpyruvate (3) (avec régénération de NaOEt). La seconde étape consiste en une réduction/cyclisation en présence de zinc dans l'acide acétique pour former du 2-carboxy-indole (4). Celui-ci peut être décarboxylé par simple chauffage pour former l'indole (5).
Notes et références
- Reissert, A. Ber. 1897, 30, 1030.
- Noland, W. E.; Baude, F. J. Organic Syntheses, Coll. Vol. 5, p.567 (1973); Vol. 43, p.40 (1963). (Article)
- Johnson, J. R.; Hasbrouck, R. B.; Dutcher, J. D.; Bruce, W. F. J. Am. Chem. Soc. 1945, 67, 423.
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Reissert indole synthesis » (voir la liste des auteurs)
- Reissert, A. Chemische Berichte 1897, 30, 1030.
Voir aussi
Catégorie :- Réaction formant un indole
Wikimedia Foundation. 2010.