- Oxyde de césium
-
Oxyde de césium 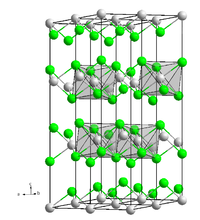
__ O2- __ Cs+
Maille cristalline de l'oxyde de césium Cs2OGénéral Nom IUPAC Oxyde de dicésium No CAS No EINECS PubChem SMILES InChI Apparence solide hygroscopique jaune orangé Propriétés chimiques Formule brute Cs2O [Isomères] Masse molaire[1] 281,8103 ± 0,0003 g·mol-1
Cs 94,32 %, O 5,68 %,Propriétés physiques T° fusion 490 °C Masse volumique 4,65 g·cm-3 Unités du SI & CNTP, sauf indication contraire. Un oxyde de césium est un composé inorganique d'oxygène et de césium. Le plus courant de ces composés a pour formule brute Cs2O, mais les oxydes binaires Cs11O3, Cs4O et Cs7O existent également[2]. Oxydes et suboxydes sont tous vivement colorés. L'oxyde de dicésium Cs2O forme des cristaux jaune orangé[3] hygroscopiques qui donnent de l'hydroxyde de césium (CsOH) au contact de toute trace d'humidité :
L'oxyde de césium est réduit par le magnésium en césium élémentaire avec formation d'oxyde de magnésium[4],[5] :
L'oxyde de césium est utilisé pour détecter les rayonnements infrarouges dans les photocathodes de dispositifs tels que des amplificateurs de lumière, des photodiodes à vide, des photomultiplicateurs et des caméras vidéo.
Notes et références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- (en) A. Simon, « Group 1 and 2 Suboxides and Subnitrides — Metals with Atomic Size Holes and Tunnels », dans Coord. Chem. Rev. 163, p. 253–270, 1997. DOI:10.1016/S0010-8545(97)00013-1.
- (en) David R. Lide, « CRC Handbook of Chemistry and Physics » 87e édition, pp. 451, 514, CRC Press, Boca Raton, Floride, États-Unis, 2006. (ISBN 0-8493-0487-3).
- (en) Francis M. Turner Jr., « The Condensed Chemical Dictionary », p. 121, Chemical Catalog Co., New York, 1920.
- (en) M. G. Arora, « S-Block Elements », p. 13, Anmol Publications, New Delhi, 1997. (ISBN 9788174885623).
