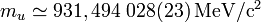- Unité atomique
-
Unité de masse atomique
L'unité de masse des atomes unifiée (symbole u ou uma, en anglais : Atomic mass unit - AMU) est une unité de mesure standard, utilisée pour mesurer la masse des atomes et des molécules.
Sommaire
En physique
Cette unité n'appartient pas au système international (SI), et sa valeur est obtenue expérimentalement. Elle est définie comme 1/12 de la masse d'un atome du nucléide 12C (carbone), non lié, au repos, et dans son état fondamental. En d'autres termes un atome de 12C a une masse de 12 u et si on prend N (nombre d'Avogadro) atomes de 12C (1 mole d'atomes), on aura une masse de 12 g ; en conséquence une u ou une uma vaut approximativement 1,66054 × 10-27 kg [1].
Autre correspondance utile (en chimie) : 1 u × N = 1 g, où N est le nombre d'Avogadro. Autrement dit, la valeur de l'unité de masse atomique exprimée en grammes correspond à l'inverse du nombre d'Avogadro.
Valeur
Dans les unités SI, le CODATA de 2006 recommande la valeur suivante :
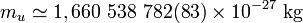 ,
,
Soit une incertitude relative de 5,0×10-8, ou bien 5,0×10-6%.
En physique nucléaire, il est plus pratique d'exprimer la masse en eV/c². Le Particle Data Group recommande en 2008[2] la valeur suivante :
En biochimie
Dans le domaine de la biochimie, on appelle également l'unité de masse des atomes le dalton (symbole Da), en l'honneur de John Dalton pour son travail sur la théorie atomique.
Un dalton est défini comme égal à 1/12e de la masse d'un atome de carbone 12, masse qui s'avéra ensuite estimée à partir d'un mélange de plusieurs isotopes (principalement carbone-12 et carbone-13, possédant respectivement 6 et 7 neutrons en sus des 6 protons de tout atome de carbone). Un dalton est, avec une assez bonne précision, la masse d'un atome d'hydrogène, la valeur exacte étant 1,00794 uma.
Le kilodalton (kDa) est beaucoup plus utilisé que le dalton en biologie et biochimie, du fait de la taille des molécules étudiées, pouvant contenir plusieurs milliers, voire millions d'atomes. À titre de repère grossier, la plupart des molécules cellulaires ont typiquement une masse comprise entre 20 et 100 kDa. Un acide aminé de protéine représente environ 110 Da, une base d'ADN (avec le désoxyribose et le phosphate, soit un nucléotide) environ 330 Da.
En chimie
En chimie, on s'intéresse peu aux masses des atomes. On préfère utiliser la masse molaire qui est la masse d'une mole d'atome.
Référence
- ↑ Site du BIPM (fichier pdf)
- ↑ Particle Physics Booklet
- Portail de la physique
- Portail de la chimie
Catégories : Unité de chimie | Unité de masse | Physique nucléaire
Wikimedia Foundation. 2010.