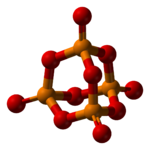
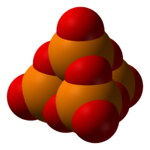
- Pentoxyde de phosphore
-
Pentoxyde de phosphore 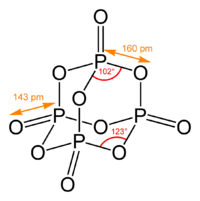
Général No CAS No EINECS Apparence cristaux blancs, hygroscopiques ou poudre[1]. Propriétés chimiques Formule brute P2O5
ou P4O10Masse molaire[2] 141,9445 ± 0,0015 g·mol-1
O 56,36 %, P 43,64 %,
283,889 g mol-1 (P4O10)Propriétés physiques T° fusion 340 °C[1] T° ébullition Point de sublimation : 360 °C[1] Solubilité dans l'eau : réaction[1] Masse volumique 2,4 g·cm-3[1] Précautions Directive 67/548/EEC 
CPhrases R : 35, Phrases S : (1/2), 22, 26, 45, Transport - 1807 SIMDUT[3] 

SGH[4] 
DangerUnités du SI & CNTP, sauf indication contraire. Le pentoxyde de phosphore est l'oxyde de phosphore longtemps vu de formule P2O5 (ce qui explique son nom) mais dont la formule brute correcte est P4O10 (dimère). C'est un composé fortement hygroscopique qui se transforme en acide phosphorique en s'hydratant, car il en est l'anhydride.
Sommaire
Utilisations
Le pentoxyde de phosphore est utilisé comme très puissant déshydratant, par exemple pour la synthèse d'anhydride d'acide à partir d'acides carboxyliques selon R − COOH + R' − COOH = R − CO − O − CO − R' + H2O Il ne peut cependant être utilisé que si les chaînes carbonées R sont suffisamment simples. En effet on obtient lors de cette synthèse de l'acide phosphorique comme sous-produit. Le pentaoxyde de phosphore est aussi utilisé comme desséchant dans les dessiccateurs
Voir aussi
Notes et références de l'article
- PENTOXYDE DE DIPHOSPHORE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- « Pentoxyde de phosphore » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
Articles connexes
Liens et documents externes
Catégories :- Composé du phosphore
- Produit chimique corrosif
- Oxyde
Wikimedia Foundation. 2010.