- Oxyde de lithium
-
Oxyde de lithium 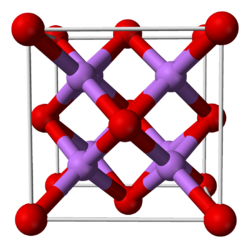
Général No CAS No EINECS Apparence poudre Propriétés chimiques Formule brute Li2O [Isomères] Masse molaire[1] 29,881 ± 0,004 g·mol-1
Li 46,46 %, O 53,54 %,Propriétés physiques T° fusion 1 570 °C Solubilité Hydrolyse violente en LiOH Masse volumique 2 013 kg·m-3 Cristallographie symbole de Pearson  [2]
[2]Classe cristalline ou groupe d’espace Fm3m (n°225) [2] Strukturbericht C1[2] Structure type CaF2 [2] Précautions Directive 67/548/EEC 
CPhrases R : 34, Phrases S : 26, 36/37/39, 45, SIMDUT[3] 
Unités du SI & CNTP, sauf indication contraire. L'oxyde de lithium est un composé chimique de formule Li2O. Il se forme avec de petites quantités d'hydroxyde de lithium LiOH lorsque le lithium métallique brûle dans l'air et se combine avec l'oxygène et l'eau atmosphériques :
- 4 Li + O2 → 2 Li2O
- 4 Li + 2 H2O + O2 → 4 LiOH
L'oxyde de lithium présente à l'état solide une structure cristalline calquée sur celle du fluorure de calcium CaF2. A l'état gazeux fondamental, la molécule Li2O est linéaire, contrairement aux résultats prévus par la théorie VSEPR (d'après laquelle la molécule Li2O devrait avoir la même forme que la molécule d'H2O), ce qui est cohérent avec une géométrie gouvernée par les liaisons ioniques.
Li2O résulte de la décomposition thermique du peroxyde de lithium Li2O2 et attaque la silice à température élevée.
Références
- Masse molaire calculée d’après Atomic weights of the elements 2007 sur www.chem.qmul.ac.uk.
- The Fluorite (C1) Structure sur http://cst-www.nrl.navy.mil/. Consulté le 17 décembre 2009
- « Oxyde de lithium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
Catégories :- Composé du lithium
- Produit chimique corrosif
- Oxyde
Wikimedia Foundation. 2010.
