Liaison σ
- Liaison σ
-
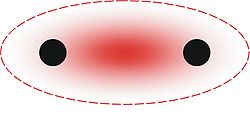
Liaison σ entre deux atomes : localisation de la densité électronique.
La liaison σ est une liaison chimique covalente qui est créée entre deux atomes par recouvrement axial d'orbitales. Il peut s'agir d'orbitales de type s ou s hybridées, mais aussi d'orbitales pz et dz² (l'axe z étant l'axe de la liaison). Les lobes des deux orbitales en interaction pointent l'une vers l'autre, contrairement au cas des liaisons π (recouvrement latéral).
Dans le cas des molécules diatomiques homonucléaires le concept de liaison σ est équivalent à celui d'orbitale moléculaire σ. Dans cette dernière, la répartition de la densité électronique a une symétrie cylindrique autour de l'axe interatomique. Parler de liaisons σ pour les molécules plus complexes est une approximation parce qu'en fait la répartition des électrons dans la molécule est définie par des orbitales moléculaires délocalisées sur l'ensemble des atomes constituant la molécule.
Les liaisons σ sont les liaisons covalentes les plus fortes (car le recouvrement axial est plus important que le recouvrement latéral), et il ne peut exister qu'une seule liaison σ entre deux atomes, si des liaisons supplémentaires sont créées, elles sont plus faibles et sont du type liaison π.
Par exemple, l'énergie de dissociation d'une liaison C-C, de type σ, est de 348 kJ.mol-1, tandis que l'énergie de dissociation de la liaison π de C=C est de 250 kJ.mol-1.
Articles connexes
Wikimedia Foundation.
2010.
Contenu soumis à la licence CC-BY-SA. Source : Article Liaison σ de Wikipédia en français (auteurs)
Regardez d'autres dictionnaires:
Liaison — Liaison … Deutsch Wörterbuch
liaison — [ ljɛzɔ̃ ] n. f. • 1190 « façon de s habiller »; de lier, ou lat. ligatio I ♦ (Choses) Action de lier, de se lier; ce qui est lié; ce qui lie. 1 ♦ (1538; sens génér.) Vx Assemblage. ♢ (1393) Mod. Opération qui consiste à incorporer des… … Encyclopédie Universelle
Liaison Pi — Liaison π La liaison π est une liaison chimique covalente qui est créée entre deux atomes par recouvrement d orbitales de nombre quantique secondaire > 1 (orbitales p, d…). Le recouvrement est latéral, c est à dire que les 2 lobes des deux… … Wikipédia en Français
Liaison pi — Liaison π La liaison π est une liaison chimique covalente qui est créée entre deux atomes par recouvrement d orbitales de nombre quantique secondaire > 1 (orbitales p, d…). Le recouvrement est latéral, c est à dire que les 2 lobes des deux… … Wikipédia en Français
Liaison Π — La liaison π est une liaison chimique covalente qui est créée entre deux atomes par recouvrement d orbitales de nombre quantique secondaire > 1 (orbitales p, d…). Le recouvrement est latéral, c est à dire que les 2 lobes des deux orbitales en… … Wikipédia en Français
liaison — Liaison. subst. feminin verb. Union, jonction de plusieurs corps ensemble. L Humide, selon l opinion commune, fait la liaison des parties qui composent le corps naturel. ces pieces sont si bien jointes qu on n en voit pas la liaison. la liaison… … Dictionnaire de l'Académie française
Liaison Δ — Formation d une lisaion δ par superposition de deux orbitales d. Une liaison (delta) est une liaison chimique covalente où 4 lobes d une orbitale occupée par un seul électron se recouvrent … Wikipédia en Français
Liaison Σ — entre deux atomes : localisation de la densité électronique. La liaison σ est une liaison chimique covalente qui est créée entre deux atomes par recouvrement axial d orbitales. Il peut s agir d orbitales de type s ou s hybridées, mais aussi… … Wikipédia en Français
Liaison C-C — Liaison carbone carbone Une liaison carbone carbone est une liaison covalente entre deux atomes de carbone[1]. La forme la plus courante est la liaison simple qui engage deux électrons, un de chaque atome. La liaison simple est une Liaison σ… … Wikipédia en Français
Liaison 3c-2e — Liaison à trois centres et deux électrons La liaison à trois centres et deux électrons, abrégée en liaison 3c 2e, est un modèle de description d une liaison chimique à déficit d électrons dans laquelle trois atomes se partagent deux électrons.… … Wikipédia en Français

