- Hydrate De Méthane
-
Hydrate de méthane
 Combustion d’hydrate de méthane (USGS).
Combustion d’hydrate de méthane (USGS).
Cadre en haut à gauche : structure du clathrate.Un hydrate de méthane (ou clathrate de méthane) est un composé organique naturellement présent dans les fonds marins, sur certains talus continentaux, ainsi que dans le pergélisol des régions polaires. C'est un des réservoirs de carbone planétaires.
Il est réputé présent en grande quantité, mais difficilement exploitable (surtout en fond marin).
Les hydrates de méthane sont une source potentielle d’énergie fossile pour remplacer le pétrole, mais ils restent une source directe de méthane ou indirecte de CO2, deux puissants gaz à effet de serre.
Appelé familièrement « glace qui brûle » ou « glace de méthane », ce composé glacé est inflammable dès qu'il fond et en présence d'oxygène ou d'un oxydant : il s’agit en effet d’une fine « cage » de glace dans laquelle est piégé du méthane (un clathrate) issu de la décomposition de matière organique relativement récente (par rapport à celle qui a donné le pétrole et le gaz naturel) effectuée par des bactéries anaérobies.
Sommaire
Découverte
Le navire de recherche Sonne remonte en juillet 1996 de l’océan Pacifique, et d’une profondeur de 785 m, 500 kg d’hydrate de méthane [1].
La structure des hydrates de méthane
L'hydrate de méthane est formé de molécules d'eau formant des cages dodécaédriques qui piègent des molécules de gaz comme le méthane, le sulfure d'hydrogène (gaz tous deux présents dans l'hydrate remonté par le navire Sonne). Ces cages peuvent stocker de considérables quantités de gaz (par exemple 164 cm3 de méthane dans 1 cm3 d'hydrate).
Réservoirs naturels
Les hydrates de méthane sont stables à basse température et à forte pression.
Ces conditions se rencontrent dans deux milieux très différents ;
Réservoir océanique
Du méthane est stocké sous forme d'hydrates de méthane dans les sédiments océaniques profonds et au niveau des talus continentaux à des profondeurs de quelques centaines de mètre.
Réservoir continental
On trouve également des hydrates de méthane dans le permafrost des régions circumpolaires de l'Eurasie et de l'Amérique.
Inventaire
Depuis les premières estimations dans les années 1970, la quantité d'hydrate de méthane dans le réservoir océanique a été révisée à la baisse mais reste considérable. Selon une estimation récente [2], cette quantité serait comprise entre 1 et 5×1015 m3 de gaz, soit entre 0,5 et 2,5 ×1012 tonnes de carbone. La quantité d'hydrates de méthane dans le réservoir continental est moins bien connue. La surface relativement faible (10 millions de km²) occupée par le permafrost laisse supposer qu'elle est moindre que dans le réservoir océanique.
Par comparaison, les réserves connues de pétrole en 2005 étaient d'environ 2×1011 m3 (voir l'article Réserves pétrolières)
Applications
Source potentielle d'énergie
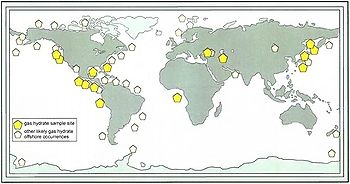 Distribution mondiales des ressources supposées ou confirmées d'hydrate de méthane, 1996.
Distribution mondiales des ressources supposées ou confirmées d'hydrate de méthane, 1996.
Source: USGSLes réserves d'hydrate de méthane sont si considérables que de nombreuses compagnies pétrolières s'y intéressent. Mais la récupération de ce composé est difficile et coûteuse, voire dangereuse pour le climat planétaire et les difficultés technologiques qui en résultent semblent actuellement loin d'être résolues.
Les Japonais, qui ont un besoin vital de nouvelles sources d'énergie, ont beaucoup investi dans le domaine, avec un programme de recherche (2001-2008) visant à localiser et qualifier les ressources sous-marines potentielles du pays, puis un plan de sept ans (« Programme sur l'exploitation de l'énergie marine et des ressources marines », voté en mars 2009. Deux extractions expérimentales devraient être faites en 2012 et en 2014 dans le secteur du « Nankai Trough » au Sud du pays où des ressources importantes ont été détectées[3],[4]Des hydrates de méthane ont déjà pu être exploités à Messoyakha (petit champ gazier peu profond de Sibérie occidentale, situé juste à la limite de stabilité des hydrates de méthane ; En conséquence, sa partie basse était un gisement de gaz "normal" (du gaz libre dans du sable) tandis que le haut était rempli d'hydrates. L'exploitation du gaz conventionnel a réduit la pression et a déstabilisé les hydrates, dont le méthane a alors pu être utilisé.
L'exploitation des hydrates de méthane pourrait poser de sérieux problèmes en matière d'effet de serre. Leur combustion émet en effet du CO2, mais pas plus que le gaz naturel (et moins que le charbon et le pétrole). Un risque est qu'en exploitant les hydrates sous-marins instables, l'on fasse involontairement remonter de grandes quantités de méthane dans l'atmosphère (cela équivaudrait à exploiter du gaz naturel avec des fuites énormes), or le méthane a un pouvoir beaucoup plus élevé que le CO2 en tant que gaz à effet de serre. Son potentiel de réchauffement global mesuré à l'échelle d'un siècle à partir de sa diffusion dans l'atmosphère est en effet compris entre 22 et 23 fois celui du dioxyde de carbone. Et cela en tenant compte d'une durée de vie moyenne des molécules de CH4 de seulement une douzaine d'années avant leur décomposition par les UV, des phénomènes de combustion ou d'oxydation, et diverses réactions chimiques.
Les industriels doivent tester en mer des méthodes de décompression des hydrates permettant de le récupérer intégralement. C'est un des projets du Japonais JOGMEC[5].Un projet allemand dit « SUGAR (acronyme signifiant Submarine Gashydrat-Lagerstätten: Erkundung, Abbau und Transport)» lancé l'été 2008 par l'Institut Leibniz pour les sciences marines de Kiel [6], sous tutelle des Ministères fédéraux de l'économie et de la technologie (BMWi) et de l'enseignement et la recherche (BMBF) avec 30 partenaires économiques et scientifiques, avec un budget initial de près de 13 millions d'euros vise à extraire du méthane marin et à stocker à sa place du CO2 capté sur des centrales thermiques ou autres installations industrielles[7].
Transport et stockage du méthane
Article détaillé : Rentabilité économique du transport du gaz naturel par la méthode NGH.L'exploitation des hydrates de méthane ne se limite pas aux fonds sous-marins. En effet, les hydrates de méthane sont une bonne alternative pour le transport du méthane sur des distances relativement longues. Ainsi, on réduirait grâce aux hydrates de méthane le transport dangereux du gaz naturel liquéfié ou encore la construction de gazoducs.
De plus, le transport des hydrates par bateau pourrait être moins coûteux en énergie que celui du gaz naturel liquéfié, car les conditions de température et de pression seraient moins difficiles à préserver que dans les méthaniers actuels.
Des recherches sont en cours de développement pour ;
- permettre de transformer le méthane gazeux en hydrates pour son transport entre le gisement et le centre de consommation.
- produire des hydrates de méthane en tant que stock d'hydrogène susceptible d'être utilisé dans des piles à combustibles
- maîtriser la formation d'hydrates de méthane dans les gazoducs où ces hydrates peuvent boucher des canalisation et/ou les endommager lorsqu'ils dégèlent. À cette fin, des biologistes tentent de comprendre comment certains organismes vivant peuvent inhiber la production de ces hydrates[8].
- transposer au CO2 des technologies proches de celles qui pourraient être développées pour les hydrates de méthane, avec l'idée de pouvoir « emprisonner » le CO2 dans de la glace (comme le méthane) et former ainsi des hydrates de CO2. Ceci pourrait peut-être permettre de garder sous pression les gisements sous-marins d'hydrates de méthane s’ils deviennent exploitables, et ainsi limiter aussi le dégagement du CO2 dans l'atmosphère.
Hydrates de méthane et changement climatique
On craint que le réchauffement climatique puisse suffisamment élever la température du pergélisol pour que les clathrates qui y sont présents fondent au moins partiellement, ce qui relâcherait énormément de méthane dans l'atmosphère, lequel viendrait à son tour augmenter l'effet de serre, d'où un effet d'emballement.
Hypothèses liées au triangle des Bermudes
Les hydrates de méthane sont une explication proposée pour la perte de nombreux navires dans le triangle des Bermudes [9] : la région possèderait d’importantes quantités d’hydrates de méthane peu stables, et de temps à autre, du gaz serait relâché. Si un navire se trouve par malchance à cet endroit pendant une éruption, il se retrouve dans de l’eau mousseuse et ne flotte plus ; il coule alors à pic en raison de la flottaison qui s’en trouve diminuée. Cette force de flottaison équivaut au poids de liquide déplacé sous la ligne de flottaison du navire. Si le liquide est mousseux, sa densité est diminuée, donc le navire doit s’enfoncer en-dessous de sa ligne de flottaison normale, et il finit par couler s’il s’enfonce au-delà de la limite de la coque.
De plus, il a été expérimenté qu’un faible taux de méthane dans l’air, de l’ordre de 1 % à 3 % est suffisant pour faire étouffer un moteur d’avion à pistons, ce qui pourrait expliquer la disparition d’avions dans cette zone : ils seraient passés au travers des émanations de méthane provenant de la mer. Il reste à savoir si l’effet est le même pour un moteur à réaction. [10].
Les démonstrations scientifiques manquent pour conforter ces hypothèses.
Voir aussi
Références
- ↑ (fr) Archimède : Énergie des abysses, émission du 26 octobre 1999, sur Arte.tv.
- ↑ A.V. Milkov, 2004, Global estimates of hydrate-bound gas in marine sediments: how much is really out there?, Earth-Sci. Rev., vol. 66, n° 3-4, p. 183-197.
- ↑ H. Saito et N. Suzuki, Terrestria organic matter controlling gas hydrate formation in the Nankai Trough accretionary prism, offshore Shikoku, Japan - Journal of Geochemical Exploration, 95 (2007) 88-100
- ↑ Vers des expériences sous-marines d'extraction d'hydrate de méthane (Bulletin ADIT/Ambassade de France au Japon / BE Japon 501 18/05/2009)
- ↑ sit internet de JOGMEC
- ↑ IFM-GEOMAR ; Kieler Leibniz Institut für Meereswissenschaften
- ↑ Communiqué relatif au projet SUGAR
- ↑ CNRC canadien, avec Virginia Walker, biologiste de l'Université Queen's, et Peter Englezos, ingénieur chimiste de l'Université de la Colombie-Britannique, cités par le bulletin ADIT 335 de l'ambassade de France au Canada, en mai 2008
- ↑ (fr) Le Triangle des Bermudes. Un mystère résolu : l’explication est liée aux hydrates de méthane.
- ↑ Source de ce dernier paragraphe : Documentaire sur Discovery Channel.
Liens externes
- Le méthane et le destin de la Terre : les hydrates de méthane : rêve ou cauchemar? Gérard Lambert, Jérôme Chappellaz, Jean-Paul Foucher, Gilles Ramstein; préface de Édouard Bard; EDP Sciences 2006
- (fr) Les hydrates de méthane: une réserve énergétique énorme, mais une bombe écologique en puissance, département de géologie et génie géologique de l’Université Laval.
- (fr) Études sur les hydrates de gaz naturels au Canada, article publié dans le "Recorder", Canadian Society of Exploration Geophysicists.
- Portail de la chimie
- Portail de l’énergie
- Portail de l’environnement et du développement durable
Catégories : Énergie fossile | Changement climatique
Wikimedia Foundation. 2010.
