- HClO4
-
Acide perchlorique
acide perchlorique 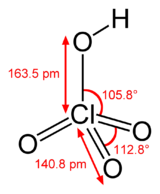
Général Nom IUPAC acide perchlorique No CAS No EINECS Apparence liquide incolore, d'odeur acre.[1] Propriétés chimiques Formule brute HClO4 [Isomères] Masse molaire 100,459 g∙mol-1
H 1 %, Cl 35,29 %, O 63,71 %,Propriétés physiques T° fusion -112 °C[1] T° ébullition (décomposition) : 19 °C[1] Solubilité dans l'eau : miscible[1] Masse volumique (eau = 1) : 1.76 à 22 °C[1] Précautions Directive 67/548/EEC 
C
OPhrases R : 5, 8, 35, Phrases S : (1/2), 23, 26, 36, 45, Transport - 1873 NFPA 704 SIMDUT[2] 


SGH[3] 

DangerUnités du SI & CNTP, sauf indication contraire. L'acide perchlorique est un oxacide à base de chlore VII de formule HClO4.
Sommaire
Description
C'est un liquide incolore, un acide fort et un oxydant fort. Ses sels sont appelés les perchlorates. C'est la seule forme du chlore stable vis à vis de la dismutation en milieu basique avec l'ion chlorure. Il peut être deshydraté en anhydride perchlorique Cl2O7 très instable.
Synthèse
On synthétise les ions perchlorates par oxydation électrochimique des ions chlorates et on obtient l'acide par action de l'acide sulfurique sur ses sels.
Utilisations
Les perchlorates sont des composés importants en pyrotechnie en tant que transporteur d'oxygène dans les mélanges. L'acide perchlorique peut être utilisé comme contre ions en solution car la majorité de ses sels sont solubles dans l'eau ce qui limite les problèmes de précipitation.
Liens externes
- (fr)Fiche INRS
- (fr)Fiche internationale de sécurité
- (en)Perchlorates dans l'alimentation aux É.-U., Environmental science & technology, 2008-02-13. (Une autre étude de la FDA donne des moyennes mais n'inclut pas les populations très exposées)
Références
- ↑ a , b , c , d et e ACIDE PERCHLORIQUE (SOLUTION A 72% ), fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Acide perchlorique » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Portail de la chimie
Catégories : Produit chimique corrosif | Produit chimique comburant | Perchlorate | Oxoacide
Wikimedia Foundation. 2010.

