- 124-04-9
-
Acide adipique
Acide adipique 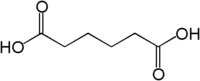
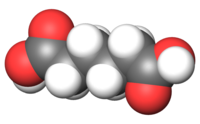
Représentations planes et 3D de l'acide adipique Général Nom IUPAC Acide hexanedioïque No CAS No EINECS No E E355 FEMA Apparence sans odeur. poudre cristalline, incolore.[1] Propriétés chimiques Formule brute C6H10O4 [Isomères] Masse molaire 146,1412 g∙mol-1
C 49,31 %, H 6,9 %, O 43,79 %,pKa pKa1: 4,43
pKa2: 5,42Propriétés physiques T° fusion 152 °C[1] T° ébullition 338 °C[1] Solubilité dans l'eau : modérée (1.4 g/100 ml à 15 °C)[1] Masse volumique (eau = 1) : 1.36[1] T° d’auto-inflammation 422 °C[1] Point d’éclair c.f. 196 °C[1] Pression de vapeur saturante à 18,5 °C : 10 Pa[1] Thermochimie ΔfH0solide -1021 kJ/mol Précautions Directive 67/548/EEC 
XiPhrases R : 36, Phrases S : (2), NFPA 704 SIMDUT[2] Produit non classifié SGH[3] 
AttentionÉcotoxicologie LogP 0.08[1] Unités du SI & CNTP, sauf indication contraire. L'acide adipique ou acide 1,6-hexanedioïque est utilisé principalement pour la fabrication du nylon, et plus généralement pour la synthèse des polyamides. C'est également un additif alimentaire (E355) utilisé pour acidifier des boissons non alcoolisées ou contrôler l’acidité des cosmétiques. Il contribue aussi au goût acide des betteraves.
Sommaire
Chimie
De formule CO2H(CH2)4CO2H, il se présente sous forme d'un solide cristallisé blanc et possède un groupe acide à ses 2 extrémités comme l’acide téréphtalique avec possibilité de développer des chaînes à chacune de ses extrémités. Par estérification avec un alcool double, tel l’éthylène glycol, il formera un polyester. Il peut également donner un polyamide.
Utilisation
Généralités
L'acide adipique est l'un des deux produits intermédiaires de base dans la fabrication du "Polyamide 6,6", encore appelé " NYLON 6,6 ". Le "Polyamide 6,6" est un produit technique dont les débouchés principaux sont l'automobile, les produits électriques, l'habillement, les produits de loisirs, … Dans un marché mondial en croissance de 3 % par an depuis 1970, la production réalisée en France représente environ 30 % de la production de l'Europe de l'Ouest (évaluée à 820 000 T par an) et induit environ 1000 emplois directs.
Procédé de fabrication et émissions de N2O
L'oxydation du mélange cyclohexanol-cyclohexanone par l'acide nitrique, conduit à une co-production d'acide adipique et de protoxyde d'azote gazeux (N₂O), dans la proportion d'environ 0,3 T N₂O pour 1T d'acide adipique.
Voir aussi
Liens externes
Références
- ↑ a , b , c , d , e , f , g , h et i ACIDE ADIPIQUE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ « Acide adipique » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Portail de la chimie
Catégories : Produit chimique irritant | Acide dicarboxylique | Monomère | Saveur acide | Régulateur alimentaire de pH
Wikimedia Foundation. 2010.

