- Dendrimère
-
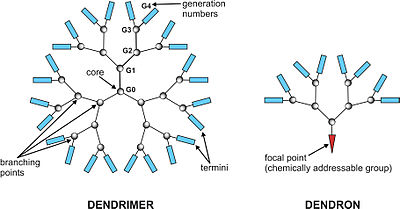
Un dendrimère [1],[2]est une molécule dont la forme reprend celle des branches d'un arbre. Le nom vient du grec "δενδρον"/dendron, signifiant "arbre". En 1979, le premier dendrimère a été synthétisé par D.A. Tomalia[3] et d'autres chercheurs de la Dow Chemical Company, et des dendrimères ont depuis été étudiés partout dans le monde pour leur forme unique.
Sommaire
Synthèse
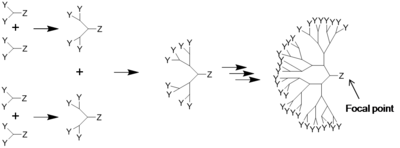
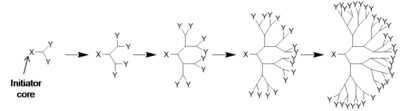
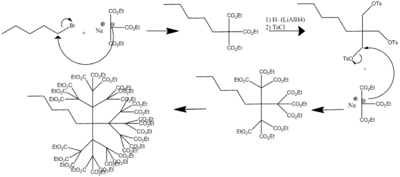
Dans la synthèse des dendrimères, les monomères mènent à un polymère monodisperse, tel un arbre[4]. Il y a deux méthodes définies de synthèse des dendrimères: synthèse divergente[5],[6] et synthèse convergente[7]. La première assemble la molécule du noyau jusqu'à la périphérie et le second de l'extérieur vers le noyau.
Cependant, parce qu'une réaction répétée composée de beaucoup d'étapes est nécessaire pour protéger l'emplacement actif, il est difficile de synthétiser des dendrimères même si les deux méthodes sont employées. C'est pourquoi il y a des obstacles à la synthèse de grandes quantités de dendrimères, toutefois de nombreux progrès ont été accomplis. Suivant les travaux de Sharpless, les méthodes "click" ont récemment permis un nouvel essor vers des voies de synthèse plus aisées et particulièrement efficaces, notamment avec des étapes de purifications simples permettant d'envisager un avenir industriel[8],[9]. Les méthodes "click" comprennent tout d'abord la réaction historique CuAAC[10] (consistant en une cycloaddition de Huisgen catalysée par du Cu(I)), mais aussi celles de Diels-Alder (DA) [11] ou le couplage Thiol-Ene (TEC)[12]. Récemment, quelques séquences employant ces trois différentes méthodes afin d'obtenir aisément des macromolécules fonctionnalisées ont vu le jour, notamment par synthèse "one-pot"[13].
Propriétés et applications
Les propriétés des dendrimères sont engendrées par les structures moléculaires présentes sur sa surface. Par exemple, un dendrimère peut être hydrosoluble quand son extrémité-groupe est un groupe hydrophile, comme un groupe carboxylique. Il est théoriquement possible de concevoir un dendrimère hydrosoluble avec l'hydrophobicité interne, qui lui permettrait de porter un composé hydrophobe dans son intérieur (afin de transporter un composé thérapeutique hydrophobe dans le sang par exemple).
Une autre propriété est que le volume d'un dendrimère augmente quand il a une charge positive. Si cette propriété peut être appliquée, des dendrimères peuvent être employés pour les systèmes de transport d'éléments chimiques qui peuvent donner le médicament à la partie visée à l'intérieur du corps d'un patient directement (tumeur par exemple).
Les applications sont très diverses comme un élément organique électroluminescent, comme substitut sanguin, traitement anti-cancer, outils pour la multiplication de cellules, mais aussi en matériaux lors d'associations avec des nanotubes ou comme sondes sélectives et efficaces.
Dendritech [14] vend actuellement un certain nombre de dendrimères de type PAMAM, ainsi que Polymer Factory[15] de type bis-MPA.
Une revue complète sur les fonctions et applications des dendrimères a été publiée en 2010 à Chemical Reviews[2].
Voir aussi
Références
- J. M. J. Fréchet, D. A. Tomalia, Dendrimers and Other Dendritic Polymers, John Wiley & Sons, Ltd. NY, NY, 2001.
- D. Astruc, E. Boisselier, C. Ornelas, « Dendrimers Designed for Functions: From Physical, Photophysical, and Supramolecular Properties to Applications in Sensing, Catalysis, Molecular Electronics, and Nanomedicine », dans Chem. Rev., vol. 110, 2010, p. 1857-1959 [lien DOI]
- D. A. Tomalia, H. Baker, J. Dewald, M. Hall, G. Kallos, S. Martin, J. Roeck, J. Ryder, P. Smith, « A New Class of Polymers: Starburst-Dendritic Macromolecules », dans Polymer (journal), vol. 17, 1985, p. 117 [lien DOI]
- Groupe Nanosciences Moléculaires et Catalyse
- Egon Buhleier, Winfried Wehner, Fritz Vögtle, « "Cascade"- and "Nonskid-Chain-like" Syntheses of Molecular Cavity Topologies », dans Synthesis, 1978, p. 155–158 [lien DOI]
- Polyphenylene Dendrimers: From Three-Dimensional to Two-Dimensional Structures Angewandte Chemie International Edition in English Volume 36, Issue 6, Date: April 4, 1997, Pages: 631-634 Frank Morgenroth, Erik Reuther, Klaus Müllen DOI:10.1002/anie.199706311
- C. J. Hawker, J. M. J. Fréchet, « Preparation of polymers with controlled molecular architecture. A new convergent approach to dendritic macromolecules », dans J. Am. Chem. Soc., vol. 112, 1990, p. 7638 [lien DOI]
- P. Antoni, Y. Hed, A. Nordberg, D. Nyström, H. von Holst, A. Hult, M. Malkoch, Bifunctional Dendrimers: From Robust Synthesis and Accelerated One-Pot Postfunctionalization Strategy to Potential Applications Angew. Int. Ed., 2009, 48 (12), pp 2126-2130 DOI:10.1002/anie.200804987
- G. Franc, A. K. Kakkar, « Click Methodologies: Efficient, Simple and Greener Routes to Design Dendrimers », dans Chemical Society Reviews, 2010 [lien DOI]
- G. Franc, A. K. Kakkar, « Dendrimers Design Using CuI-Catalyzed Alkyne–Azide "Click" Chemistry », dans Chemical Communications, 2008, p. 5267-5276 [lien DOI]
- G. Franc, A. K. Kakkar, « Diels-Alder "Click" Chemistry in Designing Dendritic Macromolecules », dans Chemistry: A European Journal, vol. 15, 2009, p. 5630-5639 [lien DOI]
- K. L. Killops, L. M. Campos, C. J. Hawker, « Robust, Efficient, and Orthogonal Synthesis of Dendrimers via Thiol-Ene "Click" Chemistry », dans J. Am. Chem. Soc., vol. 130, 2008, p. 5062-5064 [lien DOI]
- X. Q. Xiong, « Efficient Synthesis of Dendritic Architectures by One-Pot Double Click Reactions », dans Australian Journal of Chemistry, vol. 62, 2009, p. 1371 [lien DOI]
- Dendritech
- Polymer Factory AB, Stockholm, Sweden Polymer Factory
Wikimedia Foundation. 2010.