- 99393-63-2
-
Octanitrocubane
Octanitrocubane 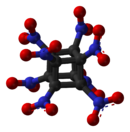
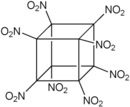
Général No CAS Propriétés chimiques Formule brute C8N8O16 [Isomères] Masse molaire 464,1296 g∙mol-1
C 20,7 %, N 24,14 %, O 55,15 %,Propriétés physiques Masse volumique 2 g/cm³ Unités du SI & CNTP, sauf indication contraire. Sommaire
Introduction
On pense que l'octanitrocubane est actuellement l'explosif le plus puissant jamais obtenu par l'homme. Paradoxalement, ce composé malgré la quantité d'énergie qu'il est capable de libérer est extêmement stable cinétiquement. On peut en effet l'écraser à coups de marteau ou le chauffer à plus de 200 °C sans provoquer d'explosion. Ceci représente un avantage considérable par rapport à des explosifs classiques tels que la nitroglycérine, le TNT ou même l'HMX.
L'inconvénient principal de ce composé est sa rareté. Sa synthèse est longue et difficile et on n'a donc pu en obtenir que quelques grammes.
Historique
L'octanitrocubane a été obtenu pour la première fois par Philip Eaton et Mao-Xi Zhang en 1999 à l'université de Chicago.1 La mise au point de sa synthèse fut particulièrement laborieuse pour un composé d'apparence aussi simple. Les dérivés du cubane sont assez délicats à manipuler à cause de la grande tension présente dans les liaisons carbone-carbone. En effet, les atomes de carbone forment habituellement des liaisons avec d'autres éléments en ménageant des angles proches de 109° entre ces liaisons. Dans le cubane et ses dérivés, ces angles sont nettement plus proches de 90°, provoquant ainsi une tension de cycle responsable de l'instabilité relative de ces molécules.
Propriétés
L'octanitrocubane est un solide blanc dont la température de fusion (avec décomposition) est bien supérieure à 200 °C.Il possède une densité de 1,98 extrêmement élevée pour un composé carboné. Sa formule brute C8N8O16 ne comporte pas d'hydrogène, ce qui est rare pour un composé organique.
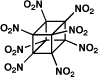 Structure chimique de l'octanitrocubane
Structure chimique de l'octanitrocubaneRéférences
Angew. Chem. Int. Ed. 2000, 39 (2), 404 - 401
Voir aussi
- Portail de la chimie
Catégories : Explosif | Nitro | Cyclobutane
Wikimedia Foundation. 2010.
