- HLA-G
-
Antigène du complexe majeur d'histocompatibilité, la molécule HLA-G, de classe I non classique, est impliquée dans la tolérance immunitaire et particulièrement dans la tolérance fœto-maternelle.
Elle est classée comme une molécule HLA non-classique de classe I parce qu'elle diffère des molécules HLA classiques de classe I par sa diversité génétique, son expression, sa structure et ses fonctions. Elle a été décrite pour la première fois avec ses applications cliniques, par Carosella Edgardo D. et son équipe à l’hôpital Saint-Louis.
De même qu'existent à la surface des globules rouges des marqueurs antigéniques qui définissent les groupes sanguins (A, B et Rhésus) et régissent les lois de la transfusion sanguine, il existe à la surface de la plupart des cellules de l'organisme des antigènes tissulaires d'histocompatibilité nommés antigènes HLA pour Human Leukocyte Antigen qui gouvernent les lois de la transplantation d’organes.
Le système des antigènes HLA est toutefois beaucoup plus complexe que celui des groupes sanguins. Les antigènes HLA sont codés par quatre types de gènes HLA-A, -B, -C et -D, qui présentent chacun un grand nombre de variantes au niveau de l'ADN (polymorphisme allélique) qui vont donner un nombre de combinaisons qui dépassent de presque trois fois le nombre d’habitants sur la terre. Ainsi, chaque individu présente à la surface de ses cellules une combinaison de molécules HLA qui lui est propre et, à l'exception des jumeaux homozygotes, chaque individu est unique et rejettera toute greffe d'organes possédant des molécules HLA différentes (situation d'histoincompatibilité).
Dans ce contexte, les neuf mois de grossesse apparaissent comme une énigme immunologique. Le fœtus qui exprime pour moitié les antigènes de la mère et pour moitié les antigènes du père, peut en effet être considéré comme une greffe semi-incompatible. Cependant, en règle générale, le fœtus est toléré par la mère durant les neuf mois de grossesse sans aucun signe de rejet. Bien qu’étroitement en contact avec les tissus maternels utérins environnants, le fœtus est isolé du système immunitaire maternel par le trophoblaste (terme utilisé au début de la grossesse puis remplacé par placenta à partir du second trimestre de grossesse) qui l’entoure. Aucun antigène HLA ne s’exprime à la surface du trophoblaste placentaire, à l’exception de HLA-G et cette expression apparaît dès le premier jour de la fécondation[1],[2].
Expression
A la différence des autres antigènes HLA-A, -B et -C dits antigènes classiques de classe I exprimés sur presque toutes les cellules nucléées de l’organisme, la protéine HLA-G, dans des situations non pathologiques, n’est exprimée qu’à la surface du cytotrophoblaste, des cellules épithéliales thymiques, de la cornée et dans le liquide amniotique. Néanmoins, la transcription de son ARNm est présente dans presque toutes les cellules de l’organisme. Cet antigène HLA joue un rôle essentiel dans la tolérance immunitaire et tout particulièrement dans la tolérance fœto-maternelle[3].
Structure
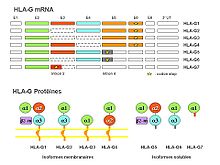
Le gène HLA-G est organisé en 8 exons séparés par 7 introns et comprend une extrémité 3’ non traduite. HLA-G diffère des autres molécules de classe I par l’absence de l’exon 7 dans son transcrit et par le fait que le codon de terminaison de traduction est localisé au niveau du deuxième codon de l’exon 6.
Il est transcrit en sept ARNm différents du fait d’un épissage alternatif[4],[5],[6], qui génèrent sept protéines différentes dont quatre sont ancrées à la membrane cellulaire (HLA-G1, -G2, -G3 et -G4) et trois sont produites sous forme de protéines solubles sécrétées par la cellule (HLA-G5, -G6 et -G7).
Le mécanisme de synthèse de protéines solubles est caractéristique du gène HLA-G et diffère des antigènes solubles classe I classiques qui sont codés par des transcrits alternatifs ayant perdu l’exon 5 du domaine transmembranaire.
La protéine HLA-G1 est de structure similaire aux antigènes HLA classiques avec 3 domaines extracellulaires α1, α2, α3 associés à la chaîne légère de la molécule de classe I, la B2 microglobuline. Sa partie cytoplasmique plus courte permet de distinguer la molécule HLA-G1 : 39kDa versus 45kDa pour les molécules HLA classiques. Les autres isoformes protéiques sont spécifiques à HLA-G et présentent la particularité d’avoir perdu 1 ou 2 domaines extracellulaires. Le transcrit HLA-G2 ne comprend pas l’exon 3, c’est-à-dire qu’il code pour une protéine dans laquelle les domaines α1 et α3 sont directement joints. Le transcrit HLA-G3 ne contient ni l’exon 3, ni l’exon 4, c’est-à-dire qu’il code pour une protéine constituée par le seul domaine α1. Le transcrit HLA-G4 ne contient pas l’exon 4, c’est-à-dire qu’il code pour une protéine dans laquelle les domaines α1 et α2 sont directement joints[7],[8].
Polymorphisme
Le polymorphisme de la molécule HLA-G est très réduit. Seules 9 variantes protéiques sont encodées par 28 allèles dont 23 correspondent à des substitutions dans la séquence codante. Néanmoins, le polymorphisme dans les régions non codantes affecte également l’expression du gène HLA-G avec une portée fonctionnelle. A cet égard, le taux et la stabilité de l’ARNm de HLA-G et l’expression de la protéine soluble par les cellules mononucléaires du sang périphérique (CMSP) sont liés au polymorphisme dans les régions régulatrices en amont de 5’ et en aval de la région 3’ non traduites du gène HLA-G. Dans les maladies humaines, les allèles de HLA-G ont été statistiquement associés aux avortements spontanés répétitifs, à la maladie inflammatoire de Bowel et à la sarcoïdose[9],[10].
Fonction Immunologique
Trois récepteurs ont été décrits pour la molécule HLA-G : ILT2/CD85j/LILRB1 (ILT2), ILT4/CD85d/LILRB2 (ILT4), et KIR2DL4/CD158d (KIR2DL4).
ILT2 est exprimé par les cellules B, les cellules T, les cellules NK, les cellules dendritiques et les macrophages. ILT4 est exprimé par les cellules dendritiques, les monocytes et les macrophages. Pour ce qui concerne KIR2DL4, son expression est principalement limitée aux sous-populations des cellules NK déciduelles et à une minorité de cellules NK périphériques. HLA-G, à travers ses récepteurs exprimés sur ces populations immunitaires, peut agir sur la plupart des fonctions du système immunitaire[11]
.
Du point de vue fonctionnel, les différentes isoformes de la molécule HLA-G inhibent l’activité cytolytique des cellules NK et des lymphocytes cytotoxiques antigènes-spécifiques CTLs[12],[13],[14], inhibent aussi la réponse proliférative allogénique des cellules T CD4+, des cellules T régulatrices et la maturation fonctionnelle des cellules dendritiques (DCS)[15],[16],[17]. L’isoforme soluble G-5 est capable d’induire aussi la différentiation des cellules T régulatrices et l’apoptose des cellules T CD8[18],[19].
Pertinence de HLA-G dans la grossesse
Au cours de la grossesse, l’expression de la molécule HLA-G dans le trophoblaste neutralise la fonction destructrice des cellules NK. L’expression de cette molécule, dite « molécule de tolérance », constitue un mécanisme d'échappement à l'immuno-surveillance et protège les cellules fœtales de l'agression des cellules immunes maternelles. Un défaut d’expression de HLA-G conduit à une rupture de la tolérance fœto-maternelle et au rejet du fœtus[20].
Pour des placentas normaux, le degré d’invasivité du trophoblaste est corrélé au niveau d’expression de HLA-G. Dans la pré-éclampsie, une pathologie de la grossesse conduisant à un avortement, il y a un déficit global d’expression protéique de HLA-G associé à une absence d’expression de l’isoforme HLA-G3. Cette altération est relié dans les profils d’expression de HLA-G à un polymorphisme de la région 3’ non traduite de l’ARNm de HLA-G.
L’expression de formes solubles de la molécule HLA-G par le tissu fœtal est indispensable à son implantation et ceci a été démontré par la corrélation entre la concentration de HLA-G soluble dans les surnageants de culture d’embryons issus de fécondation in vitro et le succès de l’implantation et de la grossesse consécutive[21],[22].
Pertinence in vivo de HLA-G en transplantation
HLA-G jouant un rôle crucial dans la tolérance fœto-maternelle, exemple physiologique parfait d’une tolérance réussie aux greffes semi-allogéniques, l’hypothèse qu’elle puisse contribuer à l’induction d’un état de tolérance en transplantation a été émise.
Le rejet d’une greffe allogénique est un événement complexe. Si les cellules potentiellement allo-réactives sont des cellules NK, elles doivent atteindre la greffe, adhérer au tissu et finalement le lyser. Cependant, si les cellules potentiellement réactives sont des lymphocytes T, une réponse allogénique doit être initiée à travers : (i) une capture et une présentation d’allo-antigènes provenant du greffon par les APCs infiltrantes ; (ii) une maturation de ces APCs ; (iii) une stimulation réciproque des lymphocytes allo-spécifique T CD4+, CD8+ et des APCs ; (iv) une migration des cellules cytolytiques vers la greffe et finalement ; (v) une lyse des cellules du greffon conduisant au rejet.
Les données in vitro indiquent que HLA-G est capable d’interférer avec chacune de ces étapes, empêchant ainsi la réaction de rejet. Son expression a été étudiée sur plus de mille patients greffés de : coeur[23], rein[24], foie-rein[25],[26] et poumon[27]. Chez ceux où HLA-G s’exprimait dans le greffon et/ou dans le plasma une acceptation sensiblement meilleure de la greffe a été constatée, avec une diminution significative du nombre d’épisodes de rejet aigu et une diminution ou absence de rejet chronique. HLA-G favorise la tolérance aux greffes d’organes.
Pertinence biologique de la molécule HLA-G en immunologie des tumeurs
Les propriétés inhibitrices de HLA-G à l’encontre des cellules immunitaires présument de la capacité des tumeurs qui expriment cette molécule à échapper à l’élimination par le système immunitaire. En effet, HLA-G exprimée par les cellules tumorales permet à ces dernières d’échapper à la destruction immunitaire en inhibant la fonction des cellules immuno-compétentes infiltrantes telles que les cellules NK, CTL et APC via l’interaction avec leurs récepteurs inhibiteurs de surface (i.e. ILT-2, ILT-4 et KIR2DL4).
HLA-G peut être exprimée à la surface des cellules tumorales ou sécrétée sous forme soluble, ou encore être incluse dans des vésicules d’exosomes sécrétées par la tumeur. Mais son expression ne concerne pas uniquement les cellules tumorales, elle est également retrouvée au niveau des cellules immunitaires infiltrant la tumeur, préférentiellement les cellules présentatrices d’antigènes[28],[29],[30],[31],[32].
Maladies infectieuses
La plupart des infections virales induisent la destruction des cellules infectées et leur élimination par le système immunitaire. Néanmoins, les virus mettent en place des stratégies d'échappement à la réponse immunitaire de l'hôte dans lesquelles HLA-G est impliquée.
Dans les infections par des virus neurotropes, deux virus, l’herpès simplex type 1 (HSV-1) et le virus de la rage (RABV) induisent l’expression neuronale de plusieurs isoformes HLA-G. Il en va de même après infection par le virus de l'immunodéficience humaine (HIV)[33].
Conclusion
La molécule HLA-G est une molécule de tolérance au sein des antigènes HLA qui sont des molécules de différence et de défense[34]. Elle joue un rôle essentiel dans la tolérance fœto-maternelle et les greffes d’organes, mais aussi dans l’échappement à l’immune surveillance de l’hôte[33] des cellules tumorales ou des cellules infectées par certains virus. La molécule HLA-G a été l’un des sujets proposés aux candidats du Baccalauréat, série S, en juin 2000.
Notes et références
- Carosella E.D., Rouas-Freiss N., Paul P., Dausset J., HLA-G: a Tolerance Molecule from the Major Histocompatibility Complex, Immunology Today, 20: 60-62, 1999
- Carosella E.D., Moreau P., LeMaoult J., Le Discorde M., Dausset J., Rouas-Freiss N., HLA-G Molecules: from Maternal-Fetal Tolerance to Tissue Acceptance, Advances in Immunology, 81: 199-252, 2003
- Carosella E.D., Favier B., Rouas-Freiss N., Moreau P., LeMaoult J., Beyond the Increasing Complexity of the Immunomodulatory HLA-G Molecule, Blood, 111: 4862-4870, 2008
- Kirszenbaum M., Moreau P., Gluckman E., Dausset J., Carosella E.D., An Alternatively Spliced Form of HLA-G mRNA in Human Trophoblasts and Evidence for the Presence of HLA-G Transcript in Adult Lymphocytes, Proc. Natl. Acad. Sci. USA, 91: 4209-4213, 1994
- Moreau Ph., Carosella E. D., Gluckman E., Gourand L., Prost S., Dausset J., Kirszenbaum M., Transcrits Différentiels du Gène du Complexe Majeur d'Histocompatibilité de Classe I non Classique HLA-G dans le Trophoblaste de 1er Trimestre de gestation et le Placenta à Terme, C.R de l'Académie des sciences de Paris, 318: 837-842, 1995
- voir aussi 2 ci-dessus
- voir aussi 1 et 2 ci-dessus
- Moreau P., Flajollet S., Carosella E.D., Non-Classical Transcriptional Regulation of HLA-G: an Update, J. Cell. Mol. Med., 13: 2973-2989, 2009
- voir aussi 8 ci-dessus
- Carosella E.D., Moreau P., LeMaoult J., Rouas-Freiss N., HLA-G: from Biology to Clinical Benefits, Trends in Immunology, 29: 125-132, 2008
- voir aussi 10 ci-dessus
- Rouas-Freiss N., Marchal R.E., Kirszenbaum M., Dausset J., Carosella E.D., The alpha1 Domain of HLA-G1 and HLA-G2 Inhibits Cytotoxicity Induced by Natural Killer Cells: Is HLA-G the Public Ligand for Natural Killer Cell Inhibitory Receptors? Proc. Natl. Acad. Sci. USA, 94: 5249-5254, 1997
- Rouas-Freiss N., Gonçalves R.M., Menier C., Dausset J., Carosella E.D., Direct Evidence to Support the Role of HLA-G in Protecting the Fetus from Maternal Uterine Natural Killer Cytolysis, Proc. Natl. Acad. Sci. USA, 94 : 11520-11525, 1997
- Riteau B., Rouas-Freiss N., Menier C., Paul P., Dausset J., Carosella E.D., HLA-G2, -G3 and -G4 Isoforms Expressed as Nonmature Cell Surface Glycoproteins Inhibit NK and Antigen-Specific CTL Cytolysis, J. Immunol., 166: 5018-5026, 2001
- LeMaoult J., Krawice-Radanne I., Dausset J., Carosella E.D., HLA-G1-Expressing Antigen-Presenting Cells Induce Immuno-Suppressive CD4+ T Cells, Proc Natl Acad Sci., 101 : 7064-7069, 2004
- Ristich V., Liang S., Zhang W., Wu J., Horuzsko A., Tolerization of Dendritic Cells by HLA-G, Eur. J. Immunol., 35: 1133–1142, 2005
- Liang S., Ristich V., Arase H., Dausset J., Carosella E.D., Horuzsko A., Modulation of Dendritic Cell Differentiation by HLA-G and ILT4 Requires the IL-6--STAT3 Signaling Pathway, Proc. Natl. Acad. Sci. USA, 105: 8357-8362, 2008
- Naji A., Le Rond S., Durrbach A., Krawice-Radanne I., Creput C., Daouya M., Caumartin J., LeMaoult J., Carosella E.D., Rouas-Freiss N., CD3+CD4low and CD3+CD8low are Induced by HLA-G: Novel Human Peripheral Blood Suppressor-T cell Subsets Involved in Transplant Acceptance, Blood, 110: 3936-3948, 2007
- voir 3 ci-dessus
- voir aussi 12 et 13
- Fuzzi B., Rizzo R., Criscuoli L., Noci I., Melchiorri L., Scarselli B., Bencini E., Menicucci A., Baricordi O.R., HLA-G Expression in early Embryos is a Fundamental Prerequisite for the Obtainment of Pregnancy, Eur. J. Immunol., 32: 311-315, 2002
- Noci I., Fuzzi B., Rizzo R., Melchiorri L., Criscuoli L., Dabizzi S., Biagiotti R., Pellegrini S., Menicucci A., Baricordi O.R., Embryonic Soluble HLA-G as a Marker of Developmental Potential in Embryos, Human Reproduction, 20: 138-146, 2005
- Lila N., Carpentier A., Amrein C., Khalil-Daher I., Dausset J., Carosella E.D., Implication of HLA-G Molecule in Heart-Graft Acceptance, The Lancet, 355: 2138, 2000
- Qiu J., Terasaki P.I., Miller J., Mizutani K., Cai J., Carosella E.D., Soluble HLA-G Expression and Renal Graft Acceptance, Am. J. Transplant., 6: 2152-2156, 2006
- Le Rond S., Azéma C., Krawice Radanne I., Durrbach A., Guettier C., Carosella E.D., Rouas-Freiss N., Evidence to Support the Role of HLA-G5 in Allograft Acceptance through Induction of Immunosuppressive/Regulatory T Cells, J. Immunol., 176: 3266-3276, 2006
- voir aussi 18 ci-dessus
- Brugière O., Thabut G., Pretolani M, Krawice-Radanne I., Dill C., Herbreteau A., Poras I., Moreau P., Colombat M., Danel C., Dehoux M., Fournier M., Carosella E.D., Rouas-Freiss N., Immunohistochemical Study of HLA-G Expression in Lung Transplant Recipients, American Journal of Transplantation, 9: 1427-1438, 2009
- Paul P., Rouas-Freiss N., Khalil-Daher I., Moreau P., Riteau B., Le Gal F.A., Avril M.F., Dausset J., Guillet J.G., Carosella E.D., HLA-G Expression in Melanoma: a Way for Tumor Cells to Escape from Immunosurveillance, Proc. Natl. Acad. Sci. USA, 95: 4510-4515, 1998
- Rouas-Freiss N., Khalil-Daher I., Riteau B., Menier C., Paul P., Dausset J., Carosella E.D., The Immunotolerance Role of HLA-G, Seminars in Cancer Biology, 9: 3-12, 1999
- Paul P., Cabestré F.A., Le Gal F.A., Khalil-Daher I., Le Danff C., Schmid M., Mercier S., Avril M.F., Dausset J., Guillet J.G., Carosella E.D., Heterogeneity of HLA-G Gene Transcription and Protein Expression in Malignant Melanoma Biopsies, Cancer Research, 59: 1954-1960, 1999
- Ibrahim E.C., Guerra N., Lacombe M.J., Angevin E., Chouaib S., Carosella E.D., Caignard A., Paul P., Tumor-Specific Up-Regulation of the Nonclassical Class I HLA-G Antigen Expression in Renal Carcinoma, Cancer Research, 61: 6838-6845, 2001
- Rouas-Freiss N., Moreau P., Menier C., LeMaoult J., Carosella E.D., Expression of Tolerognic HLA-G Molecules in Cancer Prevents Antitumor Responses, Seminars in Cancer Biol., 17: 413-421, 2007
- voir 10 ci-dessus
- Carosella E.D., Moreau P., Aractingi S., Rouas-Freiss N., HLA-G: a Shield against Inflammatory Aggression, Trends in Immunology, 22: 553-555, 2001
Voir aussi
Wikimedia Foundation. 2010.