- Effet maternel
-
En génétique du développement, un gène à effet maternel est un gène exprimé par la mère lors de l'ovogenèse. Ce type de gène est essentiellement connu par l'analyse du développement embryonnaire de Drosophila melanogaster mais aussi de Danio rerio. Les mutations à effet maternel (Dnmt, Hsf1 et Mater) ont été découvertes plus récemment chez les mammifères. Les nématodes et certaines salamandres comme les Pleurodeles ont aussi fourni des informations sur le sujet. Il se reconnaît au fait que, quel que soit son propre génotype, l'embryon exprime un phénotype correspondant uniquement au génotype de sa mère.
Sommaire
Expression
Ces gènes sont responsables, par exemple, de la forme de l'œuf avant la fécondation. On comprend dès lors qu'ils soient exprimés avant les gènes à effet zygotique. Notamment, ils polarisent l'oeuf. Des chercheurs ont ainsi démontré que l’ADN-méthyltransférase d’origine maternelle était nécessaire pour maintenir silencieux le génome zygotique et permettre ainsi les divisions cellulaires rapides qui caractérisent l’embryon de xénope. C’est également le cas chez les mammifères. Toutefois, le rôle joué par la méthylation est différent: celle-ci est notamment impliquée dans le déterminisme de l’empreinte génomique qui règle certains gènes, privilégiant l’expression d’un allèle en fonction de son origine parentale[1].
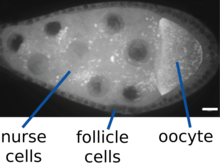
Les gènes à effet maternel sont la plupart du temps des facteurs de transcription, comme ''Bicoid'', ou d'inhibition de synthèse d'autres gènes, comme nanos. Ils sont exprimés au niveau des cellules nourricières qui entourent l’ovocyte et transportés sur un réseau polarisé de microtubules jusqu'à l'oosphère. Dans l'oosphère des moteurs moléculaires fixent l'ARNm qui leur est spécifique et le transportent le long des microtubules polarisées à un pôle de l'embryon. Ainsi Nanos et Oskar sont transportés au pôle postérieur de cette façon par des kinésines et Bicoid est quant-à lui porté au pôle antérieur par d'autres moteurs moléculaires, des dynéines. Ainsi, les ARNm sont placés uniquement à un pôle de l'embryon.
Après traduction, les protéines diffusent selon un gradient de concentration et déterminent en fonction de cette concentration la polarité antéro-postérieure et l’organisation spatiale dès le début du développement. De telles molécules sont appelées "morphogènes".
 Gradient de la protéine Bicoid dans l'embryon de drosophile
Gradient de la protéine Bicoid dans l'embryon de drosophile Gradient de la proténie Nanos dans l'embryon de drosophile
Gradient de la proténie Nanos dans l'embryon de drosophileMutations à effet maternel
On distingue deux types de mutations: les mutations à effet maternel pour lesquelles le phénotype de l'embryon dépend seulement du génotype de la mère et non du sien, et les mutations à effet zygotique, où le phénotype de l'embryon dépend de son propre génotype uniquement. Un exemple bien documenté de mutation à effet maternel concerne le gène bicoïd. Comme pour la plupart des gènes à effet maternel, il est exprimé dans les cellules nourricières dont l’ARN diffuse dans l’ovocyte où il est traduit. Le gène bicoïd détermine la région antérieure : la protéine bicoïd diffuse en effet à partir de la partie avant de l'embryon. Il s’installe ainsi un gradient de concentration de la protéine bicoïd le long de l’embryon. En fonction de la concentration, il y a activation ou répression d’autres gènes, les gènes de segmentation. Un mutant du gène bicoïd ne développe pas de structures antérieures, mais il présente deux moitiés postérieures. Ainsi, bicoïd seul permet la mise en place de la partie antérieure de l'ambryon. On dit qu'il est nécessaire et suffisant. Le gène nanos quant à lui, s'exprime selon un gradient inverse de celui de bicoïd. Il permet la formation de la partie postérieure de l'embryon de drosophile, notamment les spiracles. D'autres gènes à effet maternel connus chez la drosophile sont par exemple Gurken, Oscar, et Dorsal. Ce dernier est une protéine, et plus précisément un facteur de transcription inactivé par une protéine appelée cactus. La fixation d'un ligand sur un récepteur appelé Toll situé sur la membrane de la cellule permet à dorsal, après une réaction, de se dissocier de cactus par phosphorylation de ce dernier, et de pénétrer dans le noyau. A la suite de l'activation de Toll, qui a lieu à la face ventrale de l'embryon, il se met en place un gradient de dorsal dans le noyau. Le pourcantage de dorsal dans le noyau est corrélé au phénotype ventral que présentera ce pourcentage. Par la suite, dorsal active la transcription des gènes snail et twist et réprime les gènes ddp et zen. Or ddp et zen sont responsables de la partie dorsale de l'embryon. Ainsi, la protéine dorsal a pour effet de limiter l'expression de ddp et zen aux 40% les plus dorsaux de l'organisme[2].
Répression et activation par les gènes à effet maternel
Les gènes à effet maternel mettent en place d'autres gradients de gènes, ceux des gènes de segmentation. Ils ont notamment un effet direct sur les gap genes, qui sont des gènes ayant influant sur toute une partie des segments de l'embryon. Par exemple, bicoïd inhibe le gène ''caudal'', qui suit donc un gradient similaire à celui de nanos: il est plus important en région postérieure de l'embryon. Bicoid a aussi un rôle d'activateur vis-à-vis de Hunchback. Nanos, quant à lui, inhibe le gène hunchback. Ces deux facteurs permettent donc à Hunchback de suivre lui aussi un gradient inverse de celui de nanos et de caudal. Par la suite, Hunchback permettra la mise en place de segments thoraciques.
 Distribution des ARNm de différentes protéines le long de l'axe antéro-postérieur
Distribution des ARNm de différentes protéines le long de l'axe antéro-postérieur Gradients des différentes protéines le long de l'axe antéro-postérieur
Gradients des différentes protéines le long de l'axe antéro-postérieurBicoid a aussi des effets sur d'autres gènes. Ainsi il active d'autres gap genes, comme Giant, et inhibe Krüppel, qui a donc, tout comme Caudal, un effet sur la partie postérieure de l'embryon (segments thoraciques postérieurs et abdominaux notamment). Les gap genes, tout comme les gènes à effet maternel, agissent quant-à eux sur les gènes pair rule, ou de parité segmentaire, qui agissent sur un segment sur deux (comme Engrailed et Wingless) ainsi que sur les gènes homéotiques. Ce système est donc responsable de la mise en place de la polarité antéro-postérieure de l'embryon. En partie postérieure de l'embryon sont mis en place le telson et les spiracles, et en partie entérieure l'acron, grâce aux activations et inhibitions effectuées par les gradients de gènes à effet maternel.
Les gènes à effet maternels sont donc d'une importance capitale pour l'embryon. Ils mettent en place les axes de polarité de l'animal en activant ou réprimant d'autres gènes: les gènes de segmentation (gap, pair rule et de polérité segmentaire). Ces gènes de segmentation activent ou répriment à leur tour les gènes homéotiques, responsables de la morphologie de l'organisme.
Effet maternel environnemental
L'effet maternel peut être dû à des phénomènes épigénétiques affectant le génome de la mère en fonction de conditions expérimentales. Ainsi des chercheurs ont montré que le stress subi par la mère lors de l'ovogenèse, dû à un prédateur par exemple, pouvait avoir un effet sur la longueur des ailes et la taille des oisillons leur permettant de s'échapper plus facilement. Un phénomène épigénétique pourrait être impliqué[3].
Sources
- www.ac-reims.fr (1)
- www.ac-reims.fr (2)
- www.erudit.org
- Gènes VI, Benjamin Lewin, tarduction de la VIème édition anglaise par Isabelle Sanlaville, 1997.
- http://www.edu.upmc.fr/sdv/docs_sdvbmc/Licence/biodev/drosophile.pdf
Références
- (fr) Quand la mère est plus que responsable du devenir de sa progéniture: les mutations à effet maternel sur www.erudit.org : article de Elisabeth S. Christians, M/S : médecine sciences, Volume 19, numéro 4, p. 459-464, avril 2003. Consulté le 22 mars 2011.
- Gènes VI, Benjamin Lewin, tarduction de la VIème édition anglaise par Isabelle Sanlaville, p1186
- http://www.futura-sciences.com/fr/news/t/zoologie/d/les-oiseaux-stresses-grandissent-mieux_29111/
Voir aussi
Gène de la drosophile Gène du développement
- Portail de la biologie cellulaire et moléculaire
Wikimedia Foundation. 2010.