- XeO3
-
Trioxyde de xénon
Trioxyde de xénon 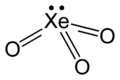

Structure du trioxyde de xénonGénéral No CAS Propriétés chimiques Formule brute XeO3 Masse molaire 179,291 g∙mol-1
O 26,77 %, Xe 73,23 %,Propriétés physiques T° fusion 25 °C (explosion) Solubilité Soluble en donnant de
l'acide xéniqueMasse volumique 4 550 kg/m3 à 15 °C Unités du SI & CNTP, sauf indication contraire. Le trioxyde de xénon est un composé instable du xénon à son état d'oxydation +6 qui se présente sous la forme d'un solide cristallin incolore. C'est un agent oxydant très puissant qui libère lentement de l'oxygène et du xénon au contact de l'eau en une réaction qui s'accélère à la lumière du soleil. C'est également un explosif dangereux au contact des matières organiques, notamment de la cellulose[1],[2].
Propriétés chimiques
Le trioxyde de xénon peut oxyder la plupart des substances oxydables, mais il réagit lentement, ce qui réduit sensiblement son intérêt comme agent oxydant[3]. En solution aqueuse, il forme une solution d'acide xénique :
- XeO3(aq) + H2O → H2XeO4
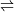 H+ + HXeO4−
H+ + HXeO4−
Cette solution est stable à la température ambiante et ne possède pas le caractère explosif du trioxyde de xénon.
Notes et références
- ↑ D. H. Templeton et al. « Crystal and Molecular Structure of Xenon Trioxide » J. Am. Chem. Soc. 85 (1963) 817
- ↑ N. Bartlett and P. R. Rao « Xenon Hydroxide: An Experimental Hazard » Science 139 (1963) 506
- ↑ N. Greenwood, A. Earnshaw, « Chemistry of the Elements », Butterworth-Heinemann (1997), Oxford
Article connexe
- Portail de la chimie
Catégories : Composé du xénon | Oxyde - XeO3(aq) + H2O → H2XeO4
Wikimedia Foundation. 2010.
