- Rapport enantiomerique
-
Excès énantiomérique
L'excès énantiomérique (abréviation ee) mesure l'énantiosélectivité d'une réaction chimique, en quantifiant, dans un milieu réactionnel ou dans un produit, la quantité de l'énantiomère dominant qui dépasse (ou excède) la quantité de l'énantiomère opposé (et qui dépasse, donc, le reste racémique du mélange):
où η + et η − désignent les fractions molaires des énantiomères dextrogyre et lévogyre, respectivement, et où η + + η − = 1.
Dans le contexte de la diastéréosélectivité, on peut définir de la même manière l'excès diastéréomérique comme étant la valeur absolue de la différence entre les quantités de deux diastéréoisomères produits dans une réaction.
Numériquement, l'excès énantiomérique est équivalent à la pureté optique (abréviation po), puisque c'est l'excès de l'énantiomère dominant qui est responsable pour l'activité optique du mélange:
où [α]obs et [α]max désignent, respectivement, l'activité optique d'un mélange d'énantiomères et l'activité optique d'un des énantiomères en état pur.
Les techniques disponibles pour mesurer un excès énantiomérique sont les mêmes que celles mesurant l'activité optique, ce qui n'identifie pas nécessairement lequel des deux énantiomères est dominant. Il est en plus possible d'évaluer l'excès énantiomérique par chromatographie sur phase chirale ou avec certaines techniques en spectroscopie RMN, ce qui évite les incertitudes dans les mesures d'activité optique et la nécessité de connaître [α]max. Puisque les diastéréoisomères auront des propriétés physiques différentes, la chromatographie simple et la spectroscopie RMN ordinaire servent à mesurer l'excès diastéréomérique.
Puisque dans la chimie moderne, l'on fait moins recours à l'activité optique pour mesurer l'excès énantiomérique, et pour simplifier le calcul des constantes d'équilibre et celui des vitesses relatives de réaction, Gawley (2006) suggère de remplacer l'utilisation des termes 'excès énantiomérique' et 'excès diastéréomérique' par l'utilisation des termes rapport énantiomérique (S:R) et rapport diastéréomérique.
Voir aussi
Bibliographie
- (en) Morrison, James D.; Mosher, Harry S.: Asymmetric Organic Reactions, Prentice-Hall, Englewood Cliff, New Jersey, 1971 (ISBN 0130495514)
- (en) International Union of Pure and Applied Chemistry (1996). "Enantiomer excess". Compendium of Chemical Terminology Internet edition.
- (en) International Union of Pure and Applied Chemistry (1996). "Optical purity". Compendium of Chemical Terminology Internet edition.
- (en) R. E. Gawley: Do the Terms "% ee" and "% de" Make Sense as Expressions of Stereoisomer Composition or Stereoselectivity? J. Org. Chem. 2006, 71(6) pp 2411 - 2416; doi:10.1021/jo052554w
Catégorie : Stéréochimie
Wikimedia Foundation. 2010.

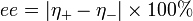
![po = \left|\frac {[\alpha]_{obs}}{[\alpha]_{max}}\right| \times 100%](/pictures/frwiki/102/ff4e9a68c2a45fe283967b733fdb227a.png)