- Opsine
-
 Pour les articles homonymes, voir Opsine (homonymie).
Pour les articles homonymes, voir Opsine (homonymie).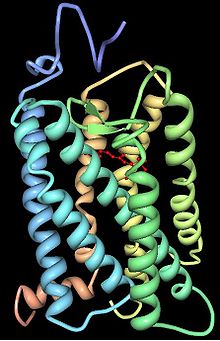 Structure spatiale de la rhodopsine bovine[1].
Structure spatiale de la rhodopsine bovine[1].
Les opsines forment une famille de protéines capables de réagir à l'énergie lumineuse grâce à sa liaison avec un chromophore particulier: le rétinal ou un de ses dérivés[2], formant ainsi une molécule mixte appelée rhodopsine. Ces protéines sont présentes dans l'ensemble du vivant, et sont impliquées dans la grande majorité des processus de photosensibilité.
On connaît bien deux catégoriés d'opsines:
- Les opsines de la bactérie Halobacterium halobium: On connaît trois opsines chez cette bactérie, qui forment, associées à un chromophore rétinoïde, la bactériorhodopsine (bR), l'halorhodopsine (hR) et la rhodopsine sensorielle (sR).
- Les opsines formant les rhodopsines visuelles, contenues dans les cellules photoréceptrices des yeux des animaux et responsables de la perception de la lumière.
Sommaire
Structure et fonction de l'opsine
L'opsine est une protéine membranaire possédant 7 hélices transmembranaires. Elle est liée à une apoprotéine dérivée de la vitamine A, le chromophore, qui peut-être soit le 11-cis-retinal, soit le 11-cis-3,4-dehydroretinal. Dans l'opsine bovine, cette liaison se fait par la lysine 296, située dans la dernière hélice transmembranaire.
L'opsine modifie la longueur d'onde d'absorption du chromophore auquel elle est associée. De plus, une fois que l'opsine est activée par l'absorption d'un photon par le chromophore, elle est capable d'activer un second messager (souvent une protéine G) et déclencher une réponse cellulaire. L'opsine confère donc à la cellule une sensibilité à la lumière.
Les opsines animales
On distingue sept grandes sous-familles d'opsines chez les animaux, qui se sont différenciées avant la séparation entre les Protostomiens et les Deutérostomiens[3].
└─o ├─o Mélanopsines / Opsines couplées à Gq └─o ├─o │ ├─o Encephalopsines / tmt-opsines │ │ │ └─o Opsines visuelles et non-Visuelles des vertébrés └─o ├─o Opsines couplées à Go └─o ├─o Neuropsines └─o ├─o Peropsines │ └─o PhotoisomérasesLes opsines des Vertébrés
La sous-famille des opsines visuelles et non-visuelles des vertébrés s'est diférenciée en 6 catégories bien distinctes, après l'individualisation de l'embranchement des Vertébrés et avant la séparation en ordre distincts[4].
└─o Pigment ancestral des Vertébrés ├─o │ ├─o Pigments P │ │ │ └─o Pigments M/LWS └─o ├─o Pigments SWS1 └─o ├─o Pigments SWS2 └─o ├─o Pigments RH2 │ └─o Pigments RH1Notes et références
- (en) Palczewski K.-2000_, « Crystal structure of Rhodopsin: A G Protein-Coupled Receptor », dans Science, vol. 289, no 5480, août 2000, p. 739-745 [lien DOI]
- Findlay, « The opsin family of proteins », dans Biochem. J., vol. 238, 1986, p. 625-642
- (en) Terakita A., « The opsins », dans Genome biology, vol. 6, no 3, mars 2005, p. 213.1-213.9 [texte intégral, lien DOI]
- S. Yokoyama, « Molecular Évolution Of Vertebrate Visual Pigments », dans Progress in Retinal and Eye Research, vol. 19, no 4, 2000, p. 385-419
Voir aussi
Articles connexes
Wikimedia Foundation. 2010.
