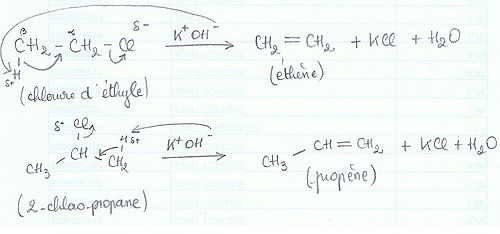- N(CH2CH3)3
-
Triéthylamine
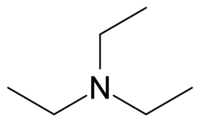
Triéthylamine Structure de la triéthylamine Général Nom IUPAC N,N-diethylethanamine
ou N,N-diethylethanamineNo CAS No EINECS FEMA Apparence liquide incolore, d'odeur caractéristique.[1] Propriétés chimiques Formule brute C6H15N [Isomères] Masse molaire 101,19 g∙mol-1
C 71,22 %, H 14,94 %, N 13,84 %,Propriétés physiques T° fusion -115 °C[1] T° ébullition 89 °C[1] Solubilité dans l'eau à 20 °C : 17 g/100 ml[1] Masse volumique 0,726 T° d’auto-inflammation 230 °C[1] Point d’éclair -17 °C (c.f.)[1] Limites d’explosivité dans l’air en volume % dans l'air : 1.2-8[1] Pression de vapeur saturante à 20 °C : 7.2 kPa[1] Précautions Directive 67/548/EEC 
C
FPhrases R : 11, 20/21/22, 35, Phrases S : (1/2), 3, 16, 26, 29, 36/37/39, 45, Transport - 1296 NFPA 704 SGH[2] 

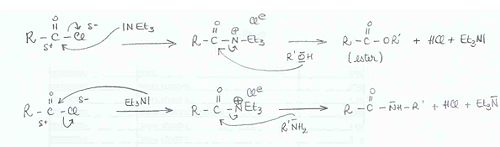
DangerÉcotoxicologie LogP 1.45[1] Unités du SI & CNTP, sauf indication contraire. La triéthylamine est un composé chimique de formule brute N(CH2CH3)3, couramment noté Et3N. On le rencontre fréquemment en synthèse organique et ce parce qu'il constitue l'amine tertiaire symétrique la plus simple, liquide à température ambiante. Il présente une forte odeur de poisson évoquant l'ammoniac. La diisopropyléthylamine est plus largement utilisée en remplacement de Et3N. Elle est communément employée en synthèse organique comme une base, spécialement dans la préparation des esters et amides à partir des chlorures d'acide.
Ces réactions conduisent à la formation d'acide chlorhydrique qui, se combinant à la triéthylamine, forment le sel d'hypochlorure de triéthylamine. Cette réaction élimine l'acide chlorhydrique du mélange, ce qui est nécessaire à la quantitativité de la réaction.
Comme les autres amines tertiaires, Et3N catalyse la formation de mousses polyuréthanes et de résines epoxy. Elle est aussi très utile dans les réactions de ß-élimination :
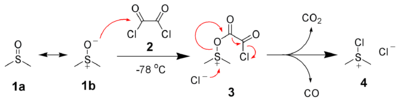
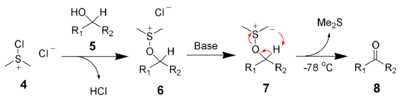
Et oxydations de Swern :
La triéthylamine s'alkyle facilement pour donner l'ammonium quaternaire correspondant :
Références
- ↑ a , b , c , d , e , f , g , h et i TRIETHYLAMINE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Portail de la chimie
Catégories : Produit chimique corrosif | Produit chimique facilement inflammable | Amine
Wikimedia Foundation. 2010.