- Quantite de matiere
-
Quantité de matière
La quantité de matière est une grandeur de comptage d'entités chimiques ou physiques. L'unité qui lui correspond est la mole.
La quantité de matière ne doit pas être confondue avec la masse qui fait référence aussi au concept énergie et qui s'exprime en kilogrammes.
Sommaire
Formules concernant les quantités de matières
Définition
La quantité de matière se définit comme suit[1]:
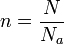
n quantité de matière (mol)
N nombre d'entités microscopiques (molecules, ions, atomes, électrons etc..)
Na constante d'Avogadro 6,02214179 x 1023 molécules = 1mol (valeur recommandée par Codata[2]).Formules dérivées
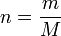
n quantité de matière (mol)
m masse de l'échantillon (g)
M masse molaire de l'espèce (masse d'une mole de cette espèce) g.mol-1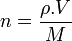
n quantité de matière (mol)
ρ masse volumique (g.cm-3)
V volume (cm3)
M masse molaire (g.mol-1)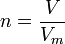 Cette relation s'applique aux gaz.
Cette relation s'applique aux gaz.
n quantité de matière
V volume de l'échantillon de gaz
Vm volume molaire (volume d'une mole de gaz dans les mêmes conditions de température et de pression que celles de l'échantillon)
Le volume molaire est employé pour les gaz. Il dépend des conditions de température et de pression. Pour un gaz parfait, ce volume ne dépend pas de la nature du gaz.
A la pression de 100 kPa (1 bar) il est égal à 22.710 980(38) dm³/mol à 0 °C et 24.789 598(42) dm³/mol à 25 °C.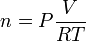
n quantité de matière (mol)
P pression (Pa "pascal")
V volume (m³)
T température (K "kelvin")
R est la constante du gaz parfait R = 8,314 472 Pa.m3.K-1.mol-1 Valeur recommandée par Codata[3]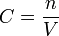
C concentration molaire (quantité de matière par unité de volume en mol.L-1)
n quantité de matière
V volumeRéférences
- ↑ IUPAC. Quantities, Units and Symbols in Physical Chemistry - the Green Book - Second Edition, Blackwell Sciences, (1993) page 41.
- ↑ CODATA value: Avogadro constant, NIST. Consulté le 2007-10-20
- ↑ CODATA value: molar gas constant, NIST. Consulté le 2007-10-20
Voir aussi
- Portail de la chimie
Catégories : Grandeur physique | Unité de chimie
Wikimedia Foundation. 2010.
