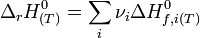- Loi de hess
-
Loi de Hess
La loi de Hessest par un principe de base de la thermochimie, élaboré par le chimiste suisse Germain Henri Hess. Elle est basée sur la propriété de l'enthalpie d'être une fonction d'état. Elle s'énonce ainsi :
- L'enthalpie de réaction d'une réaction chimique est égale à la somme des enthalpies de formation des produits, diminuée de la somme des enthalpies de formation des réactifs, en tenant compte de la stoechiométrie de la réaction.
La réaction est schématisée par la relation :
Dans les conditions standards à la température T, on obtient :
Cette loi permet, en particulier, de calculer une enthalpie de transformation impossible à obtenir directement,et en décomposant cette transformation en une suite de transformations dont les valeurs des enthalpies sont connues (voir à titre d'exemple le cycle de Born-Haber).
Exemple de calcul
Considérons la réaction de combustion du méthane
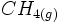 , effectuée à T sous la pression standard p°:
, effectuée à T sous la pression standard p°: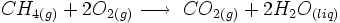
Il est possible de construire un cycle de Hess mettant en jeu la réaction précédente et des transformations impliquant les corps simples stables dans les conditions standard à T. Ce cycle est visualisé sur la figure suivante:
 Exemple d'application de la loi d'Hess.
Exemple d'application de la loi d'Hess.
Les transformations impliquant les corps simples correspondent aux réactions de formations des constituants mis en jeu dans la réaction de combustion. Comme l'enthalpie est une fonction d'état, ses variations ne dépendent pas du chemin suivi.
- On obtient:
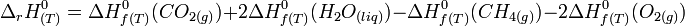
On retrouve bien la relation générale indiquée précédemment:
Remarque
- Les valeurs des enthalpies standard de formation sont données dans les tables à la température de 298 K. Elles permettent de calculer l'enthalpie standard de réaction à 298 K. La relation de Kirchhoff permet ensuite le calcul à une température différente T.
Articles connexes
- Portail de la chimie
Catégories : Thermochimie | Loi en chimie
Wikimedia Foundation. 2010.

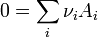 ,
,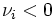 si
si 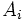 est un
est un 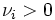 si c'est un
si c'est un