- Réseau cubique à faces centrées
-
Cubique à faces centrées
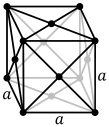
Un cristal est dit cubique à faces centrées (CFC) lorsque les nœuds de son réseau sont situés :
- aux 8 sommets d'un cube ;
- au centre de chacune des faces de ce cube.
Pour aller plus vite, les cristallographes et métallurgistes parlent parfois d'un cristal « cubique faces centrées ».
Sommaire
Structure
La maille cubique à faces centrées possède donc 8 * 1 / 8 + 6 * 1 / 2 = 4 nœuds en propre. Le mode de calcul est simple :
- les 8 nœuds aux 8 sommets sont partagés chacun entre 8 autres mailles ;
- les 6 nœuds aux centres des 6 faces du cube sont partagés chacun entre 2 mailles.
Par exemple, l'or, le cuivre et à certaines températures le fer (fer γ ou austénite) cristallisent dans une structure cfc.
Une structure formée par la copénétration de deux mailles cubiques faces centrés, la deuxième étant décalée d'une translation de a / 4, b / 4, c / 4 et qui présente donc huit atomes par maille, est nommée structure type diamant. Le carbone diamant (généralement appelé diamant), ainsi que le silicium, un des éléments les plus utilisés en tant que semi-conducteur à l'heure actuelle, cristallisent dans la structure diamant.
Paramètre de maille
En cubique faces centrées, le paramètre de la maille se déduit facilement :
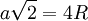 (selon la diagonale d'une face) avec R rayon de l'atome en question, d'où :
(selon la diagonale d'une face) avec R rayon de l'atome en question, d'où : 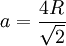
Dans le réseau cubique faces centrées, la maille simple est un rhomboèdre de paramètre :
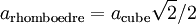 .
.Compacité
La compacité, proportion d'espace occupée par les atomes, de la maille cubique faces centrées est de :
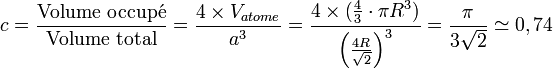
Il s'agit donc d'un assemblage compact (le plus compact avec la maille hexagonale compacte).
Sites interstitiels
La maille élémentaire cubique faces centrées comporte deux types de sites interstitiels où peut se loger, si l'espace est suffisant, un atome (en général) plus petit :
- sites tétraédriques :
Situés dans le tétraèdre formé par un atome de coin et les 3 atomes centraux des faces se coupant à ce même coin. Chaque coin est lié à un site tétraédrique, qui sont tous internes à la maille, ce qui fait 8 sites tétraédriques.
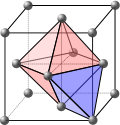
- sites octaédriques :
La maille élémentaire cubique faces centrées comporte un site octaédrique au centre de la maille, donc interne à la maille (compte pour 1). Elle comporte aussi un site au centre de chaque arête, partagé par 4 mailles, ce qui fait au total 12 x 1/4 = 3 sites. La maille élémentaire cfc comporte donc 4 sites octaédriques par maille.
- Remarques
- Des solides comme le chlorure de sodium (sel) ont une structure cristalline de type cfc où tous les sites interstitiels octaédriques sont occupés. Par exemple si l'on considère que les atomes de chlore forment la maille élémentaire cfc, les atomes de sodium occupent alors tous les sites octaédriques de la maille de chlore, et vice-versa. La totalité des sites octaédriques (4) est occupée, ce qui correspond aussi au nombre d'atome par maille, permettant ainsi de respecter la stoechiométrie. Cette structure peut être aussi vue comme deux mailles cfc imbriquées, décalées par un vecteur (1/2 ; 1/2 ; 0).
- La structure de type « diamant » est une structure de type cubique faces centrées dans laquelle 4 des 8 sites tétraédriques (2 en bas selon une diagonale et 2 en haut selon l'autre diagonale) sont occupés par des atomes de la même espèce que ceux qui composent la maille. La structure de type « blende » est du même type, à la différence que les atomes occupant les sites tétraédriques sont de nature différente (soufre pour une maille de zinc, et vice-versa, pour la sphalérite (ZnS), nom actuel de la blende). La moitié des sites tétraédriques (4) est occupée, ce qui correspond aussi au nombre d'atome par maille, permettant ainsi de respecter la stoechiométrie. La structure de type diamant peut être aussi vue comme deux mailles cfc imbriquées, décalées par un vecteur (1/4 ; 1/4 ; 1/4).
- Les hydrures métalliques utilisés pour stocker de l'hydrogène utilisent les sites tétraédriques ; en général on utilise un métal de structure cfc dans lequel sont "insérés" des atomes d'hydrogène (ils sont absorbés), qui occupent donc les sites tétraédriques, comme le palladium.
Voir aussi
- Structure cristalline
- Réseau de Bravais
- structure cubique centré
- structure diamant
- Portail des minéraux et roches
- Portail de la physique
Catégorie : Cristallographie
Wikimedia Foundation. 2010.