- Rotavirus
-
Rotavirus
Rotavirus
Légende Classification classique Règne Virus Groupe Groupe III Famille Reoviridae Genre Rotavirus Espèces de rang inférieur - Rotavirus A (RV-A)
- Rotavirus B (RV-B)
- Rotavirus C (RV-C)
- Rotavirus D (RV-D)
- Rotavirus E (RV-E)
- Rotavirus F (RV-F)
- Rotavirus G (RV-G)
Parcourez la biologie sur Wikipédia : Les Rotavirus appartiennent à la famille des Reoviridae. Le virus a été identifié en 1973 par Ruth Bishop à Melbourne.
Les rotavirus sont la 1ère cause de diarrhée aiguë sévère du jeune enfant dans le monde [1],[2].
Presque tous les enfants sont infectés par un rotavirus au cours des cinq premières années de leur vie. Cette infection peut rester asymptomatique ou entraîner une gastro-entérite (GEI = gastro-entérite infantile), dont les rotavirus sont la principale cause. L'infection est souvent asymptomatique chez l'adulte.Environ 527 000 enfants de moins de 5 ans meurent de diarrhée à rotavirus chaque année, à plus de 85% dans les pays à faible revenu d'Afrique et d'Asie [3].
Sommaire
Epidémiologie
Depuis 2001, l’OMS a mis en place un réseau de surveillance des rotavirus (réseaux régionaux de sentinelles en milieu hospitalier dans 35 pays des six régions de l'OMS), qui a montré que près de 40% des hospitalisations pour diarrhée de l’enfant de moins de 5 ans dans le monde sont dues à des rotavirus (souches G1, G2, G3, G4 et G9 le plus souvent, avec une répartition des souches variant selon les régions), ceci pour 62 584 échantillons de selles analysés. Pour ces mêmes échantillons (non nécessairement représentatifs de la réalité mondiale), pour 4 936 enfants testés positifs au rotavirus de 2001 dans les pays suivis, 325 étaient en Afrique, 388 en Amérique, 323 en Europe, 1290 en Méditerranée orientale, et 2 610 en Asie du Sud-Est et Pacifique occidental.
Les souches varient selon les pays ou les régions biogéographiques[4]Dans les pays industrialisés, les infections à rotavirus représentent 15 à 50% des cas de gastro-entérites ; bien que ces infections soient parfois sévères, la mortalité associée à celles-ci reste faible.
En France, près de 300 000 épisodes annuels seraient décomptés chez les enfants de moins de cinq ans avec une dizaine de décès ; son coût annuel est estimé à environ 28 millions d'euros.[5] Lors du pic de l'épidémie hivernale 2005–2006, on estime que 1 850 000 personnes ont consulté leur médecin généraliste en 8 semaines pour une gastro-entérite ; l'incidence a été de 367 cas pour 100 000 habitants (le seuil épidémique étant fixé à 260 cas pour 100 000 habitants)[6]. Principale cause de mortalité infantile, la gastro-entérite à rotavirus est responsable d’un demi-million de décès par an, chez les enfants de moins de cinq ans.[7]
Il s'agit donc d'un important problème de santé publique. D'autant plus que chaque année, l'épidémie de gastro-entérite à Rotavirus concorde souvent avec les épidémies de bronchiolite et de grippe, pouvant mettre en difficulté les systèmes de soins pédiatriques.[8]
On rencontre des gastro-entérites à Rotavirus lors d'épidémies hivernales, mais il existe également des cas sporadiques tout au long de l'année.
Structure
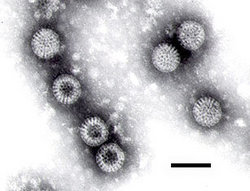
Ce sont des virus non enveloppés de structure icosaédrique et à ARN double brin (bicaténaire). En microscopie électronique, les virions de 60 à 80 nm de diamètre ont l'aspect d'une roue, d'où leur nom. Leur capside est formée de trois couches de protéines.
Leur génome est constitué de onze segments codant douze protéines. Sept groupes antigéniques ont été identifiés. La protéine VP6 de la couche intermédiaire de la capside détermine les sérogroupes, A à G. Trois d'entre eux (A, B et C) infectent les humains, majoritairement le groupe A. Les protéines de la couche externe, VP4 et VP7, induisent quant à elles, la production d'anticorps. La couche interne est formée par VP2, et les protéines VP1 et VP3 sont associées au génome.
Pathogénicité
La voie de transmission est oro-fécale directe ou indirecte, essentiellement inter-humaine. Le virus est résistant dans le milieu extérieur pendant des mois entre 4 °C à 20 °C.
La dose pathogène est estimée à environ 10 à 100 particules virales. Une personne avec une diarrhée à Rotavirus excrète un grand nombre de virus (108 - 1010 particules/ml de selles[9]) pendant environ une dizaine de jours, les doses infectieuses peuvent rapidement être acquises par les mains contaminées, les objets, les aliments, l'eau). L'excrétion asymptomatique (sans signes cliniques) est possible et peut jouer un rôle dans la persistance de cette maladie.
Très résistant au pH acide de l'estomac et aux enzymes digestives (lipases et protéases), ils infectent les cellules épithéliales matures de la muqueuse des villosités de l'intestin grêle (entérocytes). Ils les détruisent partiellement, entraînant un raccourcissement des villosités, laissant la place à des entérocytes immatures avec une diminution de l'activité enzymatique.
Une protéine non structurelle (NSP4) semblerait jouer un rôle dans la pathogénie du virus et pourrait agir comme une véritable entérotoxine virale[9].
Les virus sont ainsi « absorbés » par les cellules épithéliales digestives par endocytose dans une vésicule appelée endosome. Il semble que les protéines de la couche extérieure (VP7 et VP4) puissent rompre la membrane de l'endosome, créant ainsi un gradient de concentration en calcium. Cela facilite la fragmentation de la protéine VP7, ne laissant autour de l'ARN viral que la couche composée des protéines VP2 et VP6.
L'ARN polymérase va permettre la transcription de l'ARNm viral. Cette action est réalisée de façon plus aisée dans l'enveloppe protéinique du virus car l'environnement aqueux des cellules hôtes ralentit de façon significative le détachement des deux brins d'ARN, phase initiale de la synthèse de l'ARNm).
Le fait que l'ARN viral reste entouré, à ce stade, d'une capside est également utile pour déjouer les réponses immunitaires de l'hôte, réponses déclenchées par la présence d'un double-brin d'ARN.Au cours de l'infection, le rotavirus va donc produire un ARN messager à la fois pour la transcription des protéines, mais également pour la réplication de son génome. La plupart des protéines du rotavirus vont s'accumuler dans des structures appelées viroplasmes (structures cytoplasmiques formées au cours de l’infection) où l'ARN est répliqué.
L'infection est immunogène, protégeant d'une nouvelle infestation.
Clinique
Les rotavirus entraînent une gastro-entérite.
Après une période d'incubation allant de quelques heures à quelques jours (en général 24 à 72 heures), des selles fréquentes et liquides apparaissent soudainement. Le virus pouvant atteindre le foie, ces selles peuvent être claires et accompagnées d'urines foncées. La fièvre, généralement peu élevée, s'accompagne parfois de vomissements, surtout chez les nourrissons. La guérison complète survient après 4 à 7 jours.
Cependant, une diarrhée sévère sans réhydratation adaptée (en eau et électrolytes) peut entraîner le décès. L'association à d'autres pathogènes du système digestif peut jouer un rôle dans la sévérité de la maladie.
Les jeunes enfants, les prématurés, les personnes âgées et les sujets immunodéprimés sont particulièrement enclins à développer des symptômes plus sévères.
Diagnostic
Culture
La mise en culture du virus est difficile car nécessite un milieu particulier. En effet, il supporte mal la lumière naturelle.
Immunologie
La recherche d'antigènes viraux se fait le plus souvent par la technique ELISA (de l'anglais « Enzyme-Linked Immuno Sorbent Assay »). La technique de référence consiste à rechercher les particules virales en microscopie électronique mais n'est pas utilisée en pratique routinière de laboratoire.
Le diagnostic sérologique par recherche d'anticorps n'est pas utilisé.
Méthode moléculaire
Non utilisée en routine, elle consiste en une amplification des acides nucléiques par RT-PCR.
Facteurs favorisants ou aggravants
Ils sont représentés par une mauvaise hygiène, la vie en collectivité, l'existence d'une immunodépression.
Traitement
Il n'existe pas d'agent antiviral spécifique.
Le traitement symptomatique vise à éviter la déshydratation par une réhydratation précoce, le plus souvent orale à l'aide de solutions glycoélectrolytiques.Prévention
Règles d'hygiène
- lavage systématique des mains (après être allé à la selle, après nettoyage des fesses d'un nourrisson, avant de préparer les aliments, avant de manger) et des surfaces souillées, utilisation de solutions hydro-alcooliques.
- utilisation d'eau bouillie pour reconstituer le lait en poudre,
- éviter également de partager les verres d’eau ou les couverts à table.
Vaccin
Un premier vaccin a été développé en 1983 mais s'est révélé assez peu efficace en pratique courante dans les pays du tiers monde.
Un second vaccin oral anti-rotavirus, le Rotashield, a été breveté en 1991 et homologué en 1998 et a permis l’administration d’environ 1,5 million de doses avant l’interruption de sa commercialisation suite à une recommandation du CDC à Atlanta : quelques cas d’occlusions intestinales fatales par invagination intestinale avaient été associés à la vaccination anti-rotavirus. Ce vaccin a été élaboré à partir d’une souche de rotavirus du singe Rhésus recombinée par co-infection, avec trois souches de rotavirus humain. Les rotavirus sélectionné pour l’élaboration du vaccin possèdent dix gènes du rotavirus de singe rhésus et un gène d’une des trois souches de rotavirus humain codant la protéine VP7. Ce vaccin est efficace contre les trois sérotypes de rotavirus humain.
Depuis 2004, deux nouveaux vaccins (à virus vivants) qui ne montrent plus de risque d'occlusions intestinales fatales, lorsqu'ils sont utilisés chez le nourrisson, sont commercialisés : le Rotarix® du laboratoire GlaxoSmithKline et le Rotateq® de Merck. Administrés par voie orale, ils sont indiqués dans l’immunisation active des nourrissons à partir de 6 semaines.[10]
Deux vaccins autorisés et maintenant utilisés en routine dans 11 pays (dont Australie) ont montré une efficacité de 8 à 98% (selon les essais faits en Amérique et Europe (4,5). Ils sont testés de 2008 à 2009-2010 dans plusieurs pays pauvres pour y évaluer leur efficacité dans des contextes où leurs performances pourraient être amoindries par des souches inhabituelles de rotavirus, des infections entériques concurrentes et la malnutrition[11].
Le Conseil Supérieur d’Hygiène publique de France, section des maladies transmissibles, recommande dans un premier temps de différer la recommandation de la vaccination anti-rotavirus systématique pour les nourrissons de moins de six mois.[12]
Le CSH, Conseil Supérieur d'Hygiène belge recommandait, en février 2007, la vaccination contre le rotavirus chez tous les nourrissons à partir de l'âge de 2 mois ; aucune dose de vaccin ne sera administrée au-delà de l'âge de 6 mois vu le risque accru d'invagination intestinale observé avec un précédent vaccin contre le rotavirus chez les enfants de plus de 6 mois.
Le vaccin semble agir davantage sur la gravité de l'infection que sur son incidence.
Liens
- Fiche technique de l'Agence de Santé Publique du Canada
- Un vaccin contre le rotavirus, Roger Glass, Pour la science, 2006, 344, p 50-56
- Un vaccin contre la gastroentérite produit dans du lait de lapines transgéniques, Transgenic Research, vol 14, n°6, décembre 2005
- (en) Rotavirus (CDC)
Références et notes
- Bajolet O. Chippeaux-Hyppolite C. Rotavirus and other viruses of diarrhea. Bull Soc Pathol Exot 1998 ; 91 : 432-437.
- ↑ Parashar UD, Gibson CJ, Bresee JS, Glass RI. Rotavirus and severe childhood diarrhea. Emerg Infect Dis 2006;12:304--6.
- ↑ Parashar UD, Hummelman EG, Bresee JS, Miller MA, Glass RI. Global illness and deaths caused by rotavirus disease in children. Emerg Infect Dis 2003;9:565--72
- ↑ Parashar UD, Burton A, Lanata C, et al. World Health Organization estimates of the global mortality from rotavirus in children in the year 2004. J Infect Dis 2009 (sous presse en nov 2008).
- ↑ Gentsch JR, Laird AR, Bielfelt B, et al. Serotype diversity and reassortment between human and animal rotavirus strains: implications for rotavirus vaccine programs. J Infect Dis 2005;192:S146--59.
- ↑ Melliez H. Boelle P.Y. Baron S. Mouton Y. Yazdanpanah Y. Morbidité et coût des infections à rotavirus en France. Med et Mal Inf 2005 ; 35 (10) : 492-499.
- ↑ Sentiweb-Hebdo, Bulletin 06 du 6 au 12 février 2006, quotimed.com - 14 février 2006
- ↑ Parashar U.D. Gibson C.J. Bresee J.S. Glass R.I. Rotavirus and severe childhood diarrhea. Emerg Infect Dis 2006 ; 12 : 304-306.
- ↑ Fourquet F. Desenclos J.C. Maurage C. Baron S. Le poids médico-économique des gastro-entérites aiguës de l’enfant : l’éclairage du programme de médicalisation des systèmes d’information (PMSI). Arch Pediatr 2003 ; 10 : 861-868.
- ↑ a et b Bajolet O. Chippeaux-Hyppolite C. Rotavirus and other viruses of diarrhea. Bull Soc Pathol Exot 1998 ; 91 : 432-437.
- ↑ Le schéma de vaccination comporte :
- Soit deux doses (Rotarix®). La première dose peut être administrée à partir de l’âge de 6 semaines. L’intervalle entre les doses doit être au moins de 4 semaines. Le schéma de vaccination doit préférentiellement être administré avant l’âge de 16 semaines, et doit être terminé avant l’âge de 24 semaines ;
- Soit 3 doses (Rotateq®) : La première dose peut être administrée à partir de l’âge de 6 semaines et au plus tard à l’âge de 12 semaines. L’intervalle entre chaque dose doit être d’au moins 4 semaines. Les trois doses doivent de préférence être administrées avant l’âge de 20-22 semaines. Les 3 doses doivent être administrées avant l’âge de 26 semaines.
- ↑ Communiqué CDC : "Rotavirus Surveillance --- Worldwide, 2001--2008" (consulté 2008 111 21)
- ↑ Ministère de la Santé et des Solidarités, Direction Générale de la Santé. Avis du Conseil Supérieur d'Hygiène Publique de France, Section Maladies Transmissibles : Relatif à la vaccination anti-rotavirus chez les nourrissons de moins de six mois (séances du 22 septembre et du 5 décembre 2006) [1]
- Portail de la microbiologie
- Portail de la médecine
Catégories : Virus | Intoxication alimentaire | Infection virale | Infection de l'appareil digestif
Wikimedia Foundation. 2010.
