- P-toluidine
-
Toluidine
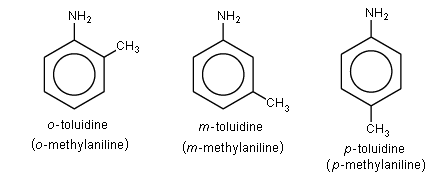
La toluidine est le nom donné à trois isomères de formule C7H9N, qui sont des composés chimiques organiques. Ces isomères sont l'o-toluidine, la m-toluidine, et la p-toluidine[1]. Toutes trois sont des amines aromatiques dont la structure chimique est similaire à celle de l'aniline sur le noyau aromatique de laquelle un groupe méthyle est substitué. La différence entre ces trois isomères est la position relative du groupe méthyle (-CH3) par rapport au groupe fonctionnel amine (-NH2);
Propriétés
Isomères de la toluidine Nom commun o-toluidine m-toluidine p-toluidine Autres noms o-méthylaniline m-méthylaniline p-méthylaniline nom chimique 2-amino-1-méthylbenzène 3-amino-1-méthylbenzène 4-amino-1-méthylbenzène Formule chimique C7H9N Masse moléculaire 107,17 g/mol Point de fusion -23 °C -30 °C 43 °C Point d'ébullition 199 à 200 °C 203 à 204 °C 200 °C Densité 1.00 g/cm³ 0.98 g/cm³ 1.05 g/cm³ N° CAS SMILES CC1=C(N)C=CC=C1 NC1=CC(C)=CC=C1 NC1=CC=C(C)C=C1 NFPA 704 SIMDUT[2],[3],[4] 



Produit non classifié SGH[5],[6],[7] 


Danger


Danger


Danger
Les propriétés chimiques des toluidines sont communes à certaines autres amines aromatiques et dans l'ensemble assez similaires à celles de l'aniline. Du fait du groupement amine lié au noyau aromatique, les toluidines sont des bases faibles. Aucune d'entre elles n'est très soluble dans l'eau pure, mais elles se neutralisent et se dissolvent dans une solution aqueuse rendue acide. De toutes émane une forte odeur aminée et, en outre, elles sont toxiques et suspectées d'être des agents cancérigènes pour l'homme.À température ambiante et pression atmosphérique, les ortho- et méta-toluidines sont des liquides visqueux tandis que la para-toluidine est un solide friable (lamelles blanc brillant). Ceci peut s'expliquer par la symétrie des molécules de p-toluidine qui peuvent, de ce fait, plus facilement s'inscrire dans une structure cristalline.
Origine et utilisations
La distillation du goudron de houille permet d'obtenir la p-toluidine, l'aniline et l'o-toluidine dans les proportions 1:1:2. L'oxydation de ce mélange à l'acide chromique par William Perkin en 1856 conduisit à la découverte de la mauvéine, le premier colorant artificiel[8]. Les toluidines sont depuis utilisées dans la productions de colorants.
Les toluidines sont également un composant des accélateurs des glues type cyanoacrylate.
La p-toluidine peut s'obtenir par réduction du p-nitrotoluène. Elle réagit sur le formaldéhyde pour former la base de Tröger.
Références & notes
- ↑ Les lettres o-, m- et p- signifient respectivement ortho-, méta- et para- et se réfèrent à la position du groupement méthyle (-CH3) par rapport à la fonction amine (-NH2).
- ↑ « Toluidine (ortho-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ « Toluidine (méta-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ « Toluidine (para-) » dans la base de données de produits chimiques Reptox de la CSST (organisme canadien responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ En anglais : Synthèse de la mauvéine ou violet d'aniline
- Portail de la chimie
Catégories : Aminobenzène | Méthylbenzène
Wikimedia Foundation. 2010.